Что такое металл и его свойства и противопоказания

Слово «металл» заимствовано из немецкого языка и окончательно усвоено в Петровскую эпоху. Первоначально имело общее значение «минерал, руда, металл», а разграничение этих понятий произошло во времена М.В.Ломоносова.
Немецкое слово «metall» произошло от латинского «metallum» — «рудник, металл».
В латинский язык слово пришло из греческого — μεταλλον: «рудник, копь».
В современном понимании, металлы — группа химических элементов, в виде простых веществ, обладающих характерными металлическими свойствами: высокая тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Однако в астрофизике термин «металл» может иметь другое значение и обозначать все химические элементы тяжелее гелия.
Как химические элементы металлы очень распространены. Из 118 химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят:
6 элементов в группе щелочных металлов,
6 в группе щёлочноземельных металлов,
38 в группе переходных металлов,
11 в группе лёгких металлов,
7 в группе полуметаллов,
14 в группе лантаноиды + лантан,
14 в группе актиноиды (физические свойства изучены не у всех элементов) + актиний,
вне определённых групп — бериллий и магний.
Таким образом, к металлам относится 96 элементов из всех открытых.
Свойства металлов
Характерные свойства металлов
Металлический блеск (характерен не только для металлов: его имеют и неметаллы иод и углерод в виде графита)
Хорошая электропроводность (из неметаллов электропроводностью обладает также углерод)
Возможность лёгкой механической обработки (см.: пластичность; однако некоторые металлы, например, германий и висмут, непластичны)
Высокая плотность (обычно металлы тяжелее неметаллов)
Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы)
Большая теплопроводность
В реакциях чаще всего являются восстановителями
Физические свойства металлов
Все металлы (кроме ртути и, условно, франция) при нормальных условиях находятся в твёрдом состоянии, однако обладают различной твёрдостью.
Температуры плавления чистых металлов лежат в диапазоне от −39°C (ртуть) до 3410°C (вольфрам). За исключением щелочных, металлы плавятся при высокой температуре, однако некоторые, например, олово и свинец, можно расплавить на обычной электрической или газовой плите.
В зависимости от плотности, металлы делят на лёгкие (плотность 0,53 ÷ 5 г/см³) и тяжёлые (5 ÷ 22,5 г/см³). Самым лёгким металлом является литий (плотность 0.53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22.6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность затруднительно: требуется полностью очистить металлы, так как любые примеси снижают их плотность.
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними. Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0,003 мм, которую используют для золочения изделий. Однако проволока из цинка или олова хрустит при сгибании, марганец и висмут почти не сгибаются, а сразу ломаются. Пластичность зависит и от чистоты металла. Очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым.
Все металлы хорошие проводники. Это обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля. Серебро, медь и алюминий имеют наибольшую электропроводность. По этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также натрий, в экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Высокая теплопроводность металлов также зависит от подвижности свободных электронов. Поэтому ряд теплопроводностей похож на ряд электропроводностей, и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла. Широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Металлы в природе. Добыча и обогащение
Источник
Говоря о положительном влиянии металлов на здоровье человека, особо выделяют золото, серебро, платину и медь. Эти металлы при лечении некоторых заболеваний просто незаменимы: к примеру, золото используют для избавления от эпилепсии, серебро полезно для почек и печени, платина оказывает успокаивающее действие, а медь может снижать давление при гипертонии.
Положительное влияние металлов на организм человека и их польза для здоровья
Лечение металлами (металлотерапия) используется с глубокой древности. С помощью серебра обеззараживали воду, солями золота лечили проказу, медь применяли при мигрени и неврозах, олово — для лечения глазных болезней. В наше время влияние металлов на здоровье смогли объяснить с научной точки зрения (хотя в этой области еще достаточно белых пятен). Одна из существующих гипотез говорит о том, что металлы и здоровье человека напрямую взаимосвязаны, а прикладывание металлических пластин к телу изменяет течение биоэлектрических токов организма. При этом происходит рефлекторное раздражение биологически активных точек, связанных с тем или иным органом.
В прошлых веках целебными металлами считались свинец, ртуть, цинк. Но они являются токсичными для организма, и их применение даже в небольшом количестве может вызвать тяжелое отравление, поэтому в настоящее время в домашнем лечении их не применяют.
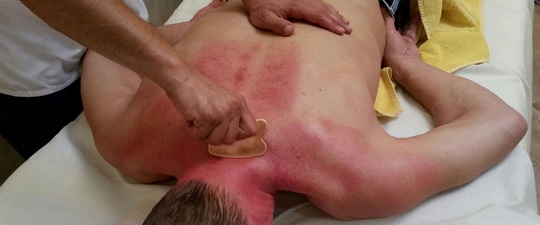
Металлы используют для лисцеления в виде пластин для аппликаций (подходят для этого монеты), оправы для камней с целебными свойствами (кольца, кулоны), браслетов. При лечении металлотерапией некоторые из них, например, серебро, применяют для очищения воды и повышения лечебных свойств настоев лекарственных растений.
Целебные металлы, влияющие на здоровье человека
Что лечат металлы и каковы полезные свойства каждого из них?
Золото — металл желтого цвета, самый мягкий и прочный из всех, оно никогда не тускнеет, легко обрабатывается. Его ценят за красоту и невосприимчивость к внешним условиям. Этот металл широко используется в промышленности, ювелирном деле и медицине.

Золото – очень полезный металл для здоровья, который обладает бактерицидными свойствами, оказывает на организм тонизирующее воздействие. Его применяют для лечения эпилепсии, при нарушениях работы сердца, упадке сил.
Противопоказано золото при заболеваниях почек, печени и сердечнососудистой системы.

Серебро — металл белого цвета. Его целебные свойства известны издавна. Еще наши предки бросали в воду серебряные монеты или украшения, чтобы обеззаразить ее. Кроме всего прочего, ионы серебра участвуют в синтезе жизненно важных ферментов в организме. Этот металл, влияющий на здоровье человека, требуется для нормальной работы желез внутренней секреции, печени, почек, мозга. С успехом этот металл используется при лечении кожных заболеваний, для ускорения сращивания костных переломов. Рекомендуется серебро и тем, у кого стойкая артериальная гипертония.
Противопоказано серебро при головокружении, беспокойном состоянии, суетливости и тревожности.

Медь — металл красного цвета. В организме человека этот микроэлемент участвует в обмене веществ, без него немыслим процесс кроветворения. Прочность нашего скелета также обеспечивается благодаря ионам меди. Положительное влияние этого металла на здоровье человека заключается и в его способности укреплять иммунитет. С лечебной целью медь применяют при болезнях желудочно-кишечного тракта, воспалительных процессах. Медные пластины, приложенные к месту ушиба, быстро снимают отек и боль. Высока польза этого металла при лечении бессонницы, психических расстройств, артериальной гипертонии и других сердечнососудистых заболеваний.
Если медная пластинка плохо удерживается на теле, значит, место аппликации выбрано неверно или металл не подходит для лечения.
При ухудшении сна, снижении настроения и появлении болей в сердце лечение следует прекратить. Противопоказаний нет.

Платина — металл серебристо-белого цвета. Полезные свойства этого металла заключаются в том, что он положительно воздействует на психическое состояние человека (успокаивает, повышает устойчивость к стрессам).
Противопоказана платина людям с выраженной неустойчивостью психики и частой сменой настроения.
Как использовать полезные свойства металлов
Наиболее популярные в народной медицине металлы — медь и серебро. Медные монеты (лучше старинные) применяют для аппликаций на больное место, прикрепляя с помощью лейкопластыря. При болях в области сердца монету приклеивают в области подключичной ямки слева на 10 дней, если это не приводит к ухудшению состояния в первые часы.
Используют влияние металлов на организм и для лечения рака. При доброкачественных опухолях матки медные монеты приклеивают к нижней части живота на 3-4 дня.
При снижении слуха одну монету прикрепляют к голове за ухом, а вторую — на лице у козелка ушной раковины на 1-2 дня.
Также воздействие металлов на организм используется при мигренях. Если у вас болит голова, нужно приложить медь к наиболее болезненному месту (лбу, вискам, затылку), и через 15-20 минут обычно наступает облегчение.
Кроме того, влияние металлов на организм человека применяют для лечения ушибов: медную монету прикрепляют лейкопластырем на 3 дня на больное место. Если она плохо держится на коже, то лечение отменяют.

Ношение браслетов из меди на руке помогает в лечении многих болезней. Они способствуют нормализации температуры тела, успокаивают нервную систему, улучшают сон, уменьшают воспалительные явления. Если от браслетов на коже не появляется покраснения, а общее состояние улучшается, значит, медь воздействует на организм положительно и лечение можно продолжить. При раздражении кожи или ухудшении самочувствия лечение прекращают.
Лечение металлами: рецепты с медной и серебряной водой
Рецепт 1
Требуется. Серебряная ложка, 800 мл воды.
Приготовление. Серебро поместить в огнеупорную емкость, залить водой и кипятить, пока ее объем не уменьшится в 2 раза.
Примечание. Использовать ежедневно для спринцеваний при кольпите. Курс лечения — 10-15 дней.
Рецепт 2
Требуется. 800 мл серебряной воды, 3 чайных ложки зеленого чая.
Приготовление. Чай залить серебряной водой, настаивать 15 минут, процедить.
Примечание. Использовать ежедневно для спринцеваний при кольпите. Курс лечения — 7-10 дней.
Рецепт 3
Требуется. 1 столовая ложка серебряной воды, 2 чайных ложки измельченной коры дуба черешчатого, 200 мл воды.
Приготовление. Кору залить водой, настаивать 6 часов, процедить и добавить серебряную воду.
Примечание. Использовать ежедневно для спринцеваний при кольпите. Курс лечения — 7-10 дней.
Рецепт 4
Требуется. 400 мл серебряной воды, 3 чайных ложки измельченных цветков ромашки аптечной.
Приготовление. Цветки залить серебряной водой, настаивать 15 минут, процедить.
Примечание. Использовать ежедневно для спринцеваний при кольпите. Курс лечения — 5-8 дней.
Рецепт 5
Требуется. 13 медных монет, по 200 мл настоя листьев крапивы двудомной (1 столовая ложка крапивы на 200 мл воды), раствора поваренной соли (1 столовая ложка на 200 мл воды).
Приготовление. Монеты положить в стакан с раствором поваренной соли на 1 час, затем обсушить.
Примечание.Болевые точки на теле при остеохондрозе смочить настоем листьев крапивы двудомной и наложить монеты. Прикрепить их полосками пластыря, оставить на 3-е суток. Через 2 дня процедуру повторить. Курс лечения -10 процедур.
Рецепт 6
Требуется. 11 серебряных монет, 200 мл настоя цветков ромашки аптечной (1 столовая ложка цветков на 200 мл воды).
Приготовление. Монеты положить на солнце на 1 час.
Примечание. Болевые точки на теле при остеохондрозе смочить отваром цветков ромашки и наложить монеты. Прикрепить их полосками пластыря и оставить на 3-е суток. Через 2 дня процедуру повторить. Курс лечения — 10 процедур.
Рецепт 7
Требуется. 4 медные монеты, 200 мл настоя цветков ромашки аптечной (1 столовая ложка цветков на 200 мл воды).
Приготовление. Монеты прокалить на сковороде 25 минут, остудить и очистить наждачной бумагой.
Примечание.Болевые точки на теле при ревматоидном артрите смочить настоем ромашки и наложить монеты. Прикрепить их полосками пластыря, оставить на 3-4 суток. Через 2-3 дня процедуру повторить. Курс лечения — 30-40 дней.
Источник
Нахождение в природе
Большая часть металлов присутствует в природе в виде руд и соединений. Они образуют оксиды, сульфиды, карбонаты и другие химические соединения. Для получения чистых металлов и дальнейшего их применения необходимо выделить их из руд и провести очистку. При необходимости проводят легирование и другую обработку металлов. Изучением этого занимается наука металлургия. Металлургия различает руды чёрных металлов (на основе железа) и цветных (в их состав не входит железо, всего около 70 элементов). Исключением можно назвать около 16 элементов: т. н. благородные металлы (золото, серебро и др.), и некоторые другие (например, ртуть, медь), которые присутствуют без примесей. Золото, серебро и платина относятся также к драгоценным металлам. Кроме того, в малых количествах они присутствуют в морской воде, растениях, живых организмах (играя при этом важную роль).
Известно, что организм человека на 3 % состоит из металлов. Больше всего в наших клетках кальция и натрия, сконцентрированного в лимфатических системах. Магний накапливается в мышцах и нервной системе, медь — в печени, железо — в крови.
Свойства металлов
Характерные свойства металлов
- Металлический блеск (кроме йода и углерода в виде графита. Несмотря на свой металлический блеск, кристаллический йод и графит относятся к неметаллам.)
- Хорошая электропроводность (кроме углерода.)
- Возможность лёгкой механической обработки (см.: пластичность; однако, некоторые металлы, например германий и висмут, непластичны.)
- Высокая плотность (обычно металлы тяжелее неметаллов.)
- Высокая температура плавления (исключения: ртуть, галлий и щелочные металлы.)
- Большая теплопроводность
- В реакциях всегда являются восстановителями
Физические свойства металлов
Все металлы (кроме ртути) тверды при нормальных условиях. Однако твёрдость их различна. Так, щелочные металлы легко режутся кухонным ножом. Сталь же по твёрдости схожа с оконным стеклом. Такие металлы, как ванадий, вольфрам и хром легко царапают самую твёрдую сталь и стекло.
Твёрдость некоторых металлов по шкале Мооса:
| Твёрдость | Металл | Обрабатываемость |
|---|---|---|
| 0.2 | Цезий | очень легко царапался бы ногтём (прикосновение опасно.) |
| 0.3 | Рубидий | очень легко царапался бы ногтём (прикосновение опасно.) |
| 0.4 | Калий | очень легко царапался бы ногтём (прикосновение опасно.) |
| 0.5 | Натрий | очень легко царапался бы ногтём (прикосновение опасно.) |
| 0.6 | Литий | очень легко царапался бы ногтём (прикосновение опасно.) |
| 1.2 | Индий | легко царапается ногтём |
| 1.2 | Таллий | легко царапается ногтём |
| 1.25 | Барий | легко царапается ногтём |
| 1.5 | Стронций | царапается ногтём |
| 1.5 | Галлий | царапается ногтём |
| 1.5 | Олово | царапается ногтём |
| 1.5 | Свинец | царапается ногтём |
| 1.5 | Ртуть | царапается ногтём (в твёрдом состоянии) |
| 1.75 | Кальций | царапается ногтём |
| 2.0 | Кадмий | царапается алюминиевой ложкой |
| 2.25 | Висмут | царапается алюминиевой ложкой |
| 2.5 | Магний | царапается медной проволокой |
| 2.5 | Цинк | царапается медной проволокой |
| 2.5 | Серебро | царапается медной монетой |
| 2.5 | Золото | царапается медной монетой |
| 3.0 | Медь | царапается кухонным ножом |
| 3.0 | Сурьма | царапается кухонным ножом |
| 3.5 | Платина | царапается кухонным ножом |
| 4.0 | Железо | царапается кухонным ножом (из нержавеющей стали) |
| 4.0 | Никель | царапается кухонным ножом (из нержавеющей стали) |
| 4.75 | Палладий | царапается кухонным ножом (из нержавеющей стали) |
| 5.0 | Кобальт | царапается стеклом и стальным гвоздём |
| 5.0 | Цирконий | царапается стеклом и стальным гвоздём |
| 5.0 | Бериллий | царапается напильником из и полевым шпатом |
| 5.5 | Молибден | царапается напильником из и полевым шпатом |
| 5.5 | Гафний | царапается напильником из и полевым шпатом |
| 6.0 | Титан | царапает стекло; царапается стеклом и напильником |
| 6.0 | Марганец | царапает стекло; царапается стеклом и напильником |
| 6.0 | Германий | царапает стекло; царапается стеклом и напильником |
| 6.0 | Ниобий | царапает стекло; царапается стеклом и напильником |
| 6.0 | Родий | царапает стекло; царапается стеклом и напильником |
| 6.5 | Рутений | царапает стекло; царапается кварцом |
| 6.5 | Тантал | царапает стекло; царапается кварцом |
| 6.5 | Иридий | царапает стекло; царапается кварцом |
| 7.0 | Ванадий | царапает все виды сталей; царапается топазом |
| 7.0 | Рений | царапает все виды сталей; царапается топазом |
| 7.0 | Осмий | царапает все виды сталей; царапается топазом |
| 7.5 | Вольфрам | царапает все виды сталей; царапается топазом |
| 8.5 | Хром | легко царапает стекло и все металлы; царапается рубином |
Температуры плавления лежат в диапазоне от −39 °C (ртуть) до 3410 °C (вольфрам). Температура плавления большинства металлов (за исключением щелочных) высока, однако некоторые «нормальные» металлы, например олово и свинец, можно расплавить на обычной электрической или газовой плите.
В зависимости от плотности металлы делят на лёгкие (плотность 0,53 ÷ 5 г/см³) и тяжёлые (5 ÷ 22,5 г/см³). Самым лёгким металлом является литий (плотность 0.53 г/см³). Самый тяжёлый металл в настоящее время назвать невозможно, так как плотности осмия и иридия — двух самых тяжёлых металлов — почти равны (около 22.6 г/см³ — ровно в два раза выше плотности свинца), а вычислить их точную плотность крайне сложно: для этого нужно полностью очистить металлы, ведь любые примеси снижают их плотность.
Большинство металлов пластичны, то есть металлическую проволоку можно согнуть, и она не сломается. Это происходит из-за смещения слоёв атомов металлов без разрыва связи между ними. Самыми пластичными являются золото, серебро и медь. Из золота можно изготовить фольгу толщиной 0.003 мм, которую используют для золочения изделий. Однако не все металлы пластичны. Проволока из цинка или олова хрустит при сгибании; марганец и висмут при деформации вообще почти не сгибаются, а сразу ломаются. Пластичность зависит и от чистоты металла; так, очень чистый хром весьма пластичен, но, загрязнённый даже незначительными примесями, становится хрупким и более твёрдым.
Все металлы хорошо проводят электрический ток; это обусловлено наличием в их кристаллических решётках подвижных электронов, перемещающихся под действием электрического поля. Серебро, медь и алюминий имеют наибольшую электропроводность; по этой причине последние два металла чаще всего используют в качестве материала для проводов. Очень высокую электропроводность имеет также натрий, в экспериментальной аппаратуре известны попытки применения натриевых токопроводов в форме тонкостенных труб из нержавеющей стали, заполненных натрием. Благодаря малому удельному весу натрия, при равном сопротивлении натриевые «провода» получаются значительно легче медных и даже несколько легче алюминиевых.
Высокая теплопроводность металлов также зависит от подвижности свободных электронов. Поэтому ряд теплопроводностей похож на ряд электропроводностей и лучшим проводником тепла, как и электричества, является серебро. Натрий также находит применение как хороший проводник тепла; широко известно, например, применение натрия в клапанах автомобильных двигателей для улучшения их охлаждения.
Гладкая поверхность металлов отражает большой процент света — это явление называется металлическим блеском. Однако в порошкообразном состоянии большинство металлов теряют свой блеск; алюминий и магний, тем не менее, сохраняют свой блеск и в порошке. Наиболее хорошо отражают свет алюминий, серебро и палладий — из этих металлов изготовляют зеркала. Для изготовления зеркал иногда применяется и родий, несмотря на его исключительно высокую цену: благодаря значительно большей, чем у серебра или даже палладия, твёрдости и химической стойкости, родиевый слой может быть значительно тоньше, чем серебряный.
Цвет у большинства металлов примерно одинаковый — светло-серый с голубоватым оттенком. Золото, медь и цезий соответственно жёлтого, красного и светло-жёлтого цвета.
Химические свойства металлов
На внешнем электронном слое у большинства металлов небольшое количество электронов (1-3), поэтому они в большинстве реакций выступают как восстановители (то есть «отдают» свои электроны)
1. Реакции с простыми веществами
- С кислородом реагируют все металлы, кроме золота, платины. Реакция с серебром происходит при высоких температурах, но оксид серебра(II) практически не образуется, так как он термически неустойчив. В зависимости от металла на выходе могут оказаться оксиды, пероксиды, надпероксиды:
4Li + O2 = 2Li2O оксид лития
2Na + O2 = Na2O2 пероксид натрия
K + O2 = KO2 надпероксид калия
Чтобы получить из пероксида оксид, пероксид восстанавливают металлом:
Na2O2 + 2Na = 2Na2O
Со среднмими и малоактивными металлами реакция происходит при нагревании:
3Fe + 2O2 = Fe3O4
2Hg + O2 = 2HgO
2Cu + O2 = 2CuO
- С азотом реагируют только самые активные металлы, при комнатной температуре взаимодействует только литий, образуя нитриды:
6Li + N2 = 2Li3N
При нагревании:
2AL + N2 = 2AlN
3Ca + N2 = 2Ca3N2
- С серой реагируют все металлы, кроме золота и платины:
Железо взаимодействует с серой при нагревании, образуя сульфид:
Fe + S = FeS
- С водородом реагируют только самые активные металлы, то есть металлы IA и IIA групп кроме Be. Реакции осуществляются при нагревании, при этом образуются гидриды. В реакциях металл выступает как восстановитель, степень окисления водорода −1:
2Na + H2 = 2NaH
Mg + H2 = MgH2
- С углеродом реагируют только наиболее активные металлы. При этом образуются ацетилениды или метаниды. Ацетилениды при взаимодествии с водой дают ацетилен, метаниды — метан.
2Na + 2C = Na2C2
Na2C2 + 2H2O = 2NaOH + C2H2
2Na + H2 = 2NaH
Легирование
Это введение в расплав дополнительных элементов, улучшающих механические, физические и химические свойства основного материала.
Микроскопическое строение
Характерные свойства металлов можно понять, исходя из их внутреннего строения. Все они имеют слабую связь электронов внешнего энергетического уровня (другими словами, валентных электронов) с ядром. Благодаря этому созданная разность потенциалов в проводнике приводит к лавинообразному движению электронов (называемых электронами проводимости) в кристаллической решётке. Совокупность таких электронов часто называют электронным газом. Вклад в теплопроводность, помимо электронов, дают фононы (колебания решётки). Пластичность обусловлена малым энергетическим барьером для движения дислокаций и сдвига кристаллографических плоскостей. Твёрдость можно объяснить большим числом структурных дефектов (междоузельные атомы, вакансии и др.).
Из-за лёгкой отдачи электронов возможно окисление металлов, что может приводить к коррозии и дальнейшей деградации свойств. Способность к окислению можно узнать по стандартному ряду активности металлов. Этот факт подтверждает необходимость использования металлов в комбинации с другими элементами (сплав, важнейшим из которых является сталь), их легирование и применение различных покрытий.
Для более корректного описания электронных свойств металлов необходимо использовать квантовую механику. Во всех твёрдых телах с достаточной симметрией уровни энергии электронов отдельных атомов перекрываются и образуют разрешённые зоны, причём зона, образованная валентными электронами, называется валентной зоной. Слабая связь валентных электронов в металлах приводит к тому, что валентная зона в металлах получается очень широкой, и всех валентных электронов не хватает для её полного заполнения.
Принципиальная особенность такой частично заполненной зоны состоит в том, что даже при минимальном приложенном напряжении в образце начинается перестройка валентных электронов, т. е. течёт электрический ток.
Та же высокая подвижность электронов приводит и к высокой теплопроводности, а также к способности зеркально отражать электромагнитное излучение (что и придаёт металлам характерный блеск).
Некоторые металлы
- Щелочные:
- Цезий
- Литий
- Натрий
- Калий
- Щёлочноземельные:
- Бериллий
- Магний
- Кальций
- Переходные
- Железо
- Платина
- Медь
- Цинк
- Золото
- Серебро
- Палладий
- Ртуть
- Никель
- Кобальт
- Другие:
- Алюминий
- Свинец
- Олово
Применение металлов
Конструкционные материалы
Металлы и их сплавы — одни из главных конструкционных материалов современной цивилизации. Это определяется прежде всего их высокой прочностью, однородностью и непроницаемостью для жидкостей и газов. Кроме того, меняя рецептуру сплавов, можно менять их свойства в очень широких пределах.
Электротехнические материалы
Металлы используются как в качестве хороших проводников электричества (медь, алюминий), так и в качестве материалов с повышенным сопротивлением для резисторов и электронагревательных элементов (нихром и т. п.).
Инструментальные материалы
Металлы и их сплавы широко применяются для изготовления инструментов (их рабочей части). В основном это инструментальные стали и твёрдые сплавы. В качестве инструментальных материалов применяются также алмаз, нитрид бора, керамика.
Wikimedia Foundation.
2010.
Синонимы:
Смотреть что такое “Металл” в других словарях:
металл — презренный металл.. Словарь русских синонимов и сходных по смыслу выражений. под. ред. Н. Абрамова, М.: Русские словари, 1999. металл хлеб индустрии Словарь русских синонимов … Словарь синонимов
МЕТАЛЛ — (греч.). Простое тело, тяжелое, непрозрачное, с более или менее сильною степенью блеска, тягучести и способности проводить теплоту и электричество. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. МЕТАЛЛ лат.… … Словарь иностранных слов русского языка
МЕТАЛЛ — МЕТАЛЛ, метал муж., лат. крушец; а в малом виде, в выплавке: королек. В быту житейском, ценные, дорогие металлы: золото, платина, серебро; простые: железо, медь, цинк, олово, свинец; химия открыла такие начала почти всех ископаемых, состоящих из… … Толковый словарь Даля
Металл — см. Ремесло … Библейская энциклопедия Брокгауза
МЕТАЛЛ — [ал], металла, муж. (греч. metallon, букв. рудник). Химически простое тело (или сплав), отличающееся блеском, ковкостью, плавкостью и способностью проводить теплоту и электричество. Черные металлы (железо, чугун, сталь и др.). Благородные или… … Толковый словарь Ушакова
МЕТАЛЛ — МЕТАЛЛ, а, муж. Химически простое вещество, обладающее особым блеском, ковкостью, хорошей теплопроводностью и электропроводностью. Чёрные металлы (железо и его сплавы). Цветные металлы (все металлы, кроме чёрных). Благородные (драгоценные)… … Толковый словарь Ожегова
металл — МЕТАЛЛ, а, м. 1. Металлический рок. 2. Деньги. Я не при металле. 1. из муз … Словарь русского арго
металлёр — сущ., кол во синонимов: 1 • металлер (3) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
металлёр — (СРСЮЮ) … Словарь употребления буквы Ё
металл — 1. Непрозрачное блестящее элементарное вещество, которое является хорошим проводником тепла и электричества и, когда отполировано, характеризуется хорошим светоотражением. Большинство металлов ковки и пластичны и отличаются большей плотностью,… … Справочник технического переводчика
Металл — (Metal) Определение металла, физические и химические свойства металлов Определение металла, физические и химические свойства металлов, применение металлов Содержание Содержание Определение Нахождение в природе Свойства Характерные свойства… … Энциклопедия инвестора
Источник
