Фторхинолоны противопоказания для детей
Комментарии
Опубликовано в журнале:
Практика педиатра
Сентябрь, 2007
С.С. Постников, профессор кафедры клинической фармакологии с курсом клинической фармакологии и фармакокинетики ФУВ ГОУ ВПО «Российский государственный медицинский университет» Росздрава, д-р мед. наук
Антимикробные препараты группы фторхинолонов (ФХ) заняли во взрослой практике одно из ведущих мест среди антибиотиков с широким диапазоном действия, используемых для лечения сепсиса, менингита, остеомиелита, брюшного тифа, муковисцидоза. Однако до сих пор не сняты ограничения на применение ФХ у детей.
Термин «фторхинолоны» (а точнее сказать «монофторхинолоны»; в данной статье речь пойдет именно о них) отражает две основные особенности химического строения этих препаратов: принадлежность к классу хинолонов и наличие в молекуле одного атома фтора. Это высокоактивные синтетические химиотерапевтические средства широкого спектра действия с фармакокинетикой, обеспечивающей высокую степень биодоступности, хорошее проникновение в органы, ткани, биологические жидкости и клетки.
Фторхинолоны в педиатрии
С начала 80-х годов XX века ФХ (ципрофлоксацин, пефлоксацин и офлоксацин) стали применяться в детской практике. Основные характеристики этих антибиотиков, привлекшие внимание педиатров:
- Высокая активность против P. aeruginosa и полирезистентных стафилококков.
- Высокие концентрации в различных органах и биологических жидкостях, что позволяет лечить инфекции любой локализации.
- Наличие двух одинаково эффективных лекарственных форм для энтерального и парэнтерального применения, создающих возможность амбулаторного лечения и ступенчатой терапии.
- Возможность двукратного приема.
- Хорошая переносимость.
Первым заболеванием, при котором ФХ были успешно использованы у детей, стал муковисцидоз (МВ). Это объясняется следующими причинами:
- Инфекции бронхолегочной системы определяют тяжесть состояния и продолжительность жизни у этих больных.
- У больных МВ имеется склонность к инфицированию мультирезистентными штаммами (P. aeruginosa) и поэтому, а также вследствие необходимости пожизненного лечения, они нуждаются в новых, более мощных антибиотиках.
- ФХ являются практически единственными препаратами для перорального приема, активными против P. aeruginosa.
- ФХ создают высокие концентрации в бронхиальном секрете, что чрезвычайно важно с учетом внутрибронхиального расположения возбудителей респираторной инфекции при МВ.
- ФХ напрямую снижают продукцию медиаторов воспаления МВ-цитокинов и активность клеток воспаления – фагоцитов.
- Продолжительность ремиссии после терапии ципрофлоксацином у больных МВ в 2 раза дольше, чем после применения аминогликозидов и антисинегнойных пенициллинов (Н.И. Капранов, 1994).
Все эти обстоятельства выдвинули на передний план ФХ, сделав их новым стандартом антибактериального лечения МВ.
Другим заболеванием, где применение ФХ у детей оправданно из-за отсутствия более эффективной альтернативы, является апластическая анемия (АА). Исследования последних лет показали, что интенсивная иммуносупрессивная терапия с использованием антитимоцитарного гормона в сочетании с циклоспорином А, метилперднизолоном и (в отдельных случаях) гранулоцитарным колониестимулирующим фактором обеспечивает высокий уровень выживаемости и гематологических ремиссий у больных АА. Однако свойственный этому заболеванию глубокий агранулоцитоз служит причиной частого (у 70% больных) развития серьезных бактериальных и грибковых инфекций, нередко с фатальным исходом.
Большинство инфекций у иммунокомпроментированных больных обычно вызывается аутофлорой, населяющей толстый кишечник. Поэтому в современные протоколы сопроводительного лечения больных АА вошли ФХ, которые используются для деконтаменации кишечника больных в период гранулоцитопении. Их преимущество перед ранее используемыми антибактериальными средствами (ванкомицин, гентамицин, ко-тримоксазол) состоит в следующем:
- ФХ создают в фекалиях концентрации, в 10–100 раз превышающие сывороточные, причем эти концентрации сохраняются в течение нескольких дней после отмены препарата, что предупреждает раннюю реинфекцию.
- После применения ФХ из фекалий полностью элиминируются псевдомонады и энтерококки, при этом ФХ не действуют на лактобациллы и бифидобактерии, составляющие основу колонизационной резистентности.
- Накапливаясь в макро- и микрофагах, ФХ не повреждают эти клетки, не удлиняют тем самым нейтропеническую фазу заболевания.
Побочные эффекты
Общая частота всех побочных эффектов ФХ колеблется в разных странах, составляя в Европе 3%, в Японии – 6,5%, в США – 13,4%, что объясняется этническими различиями, а также применением в США более высоких доз ФХ (Р. Шахт, 1989; P. Ball, 1986, 1994). Все побочные эффекты носят транзиторный характер и редко когда являются причиной отмены препарата (2,8%).
Наиболее часто (2–10%) отмечаются нежелательные реакции со стороны ЖКТ: нарушение аппетита, боли в животе, тошнота или рвота, запоры (диарея), отдельные случаи псевдомембранозного колита и дисбиоза, нарушение функции печени.
Реакции со стороны ЦНС в виде головной боли, бессонницы, кошмаров, изменения настроения, делирия, обшей слабости, асептического менингита наблюдаются у 1–4,4% больных. ФХ (чаще офлоксацин) могут быть причиной повышенной возбудимости, очень редко встречаются судорожные реакции (ципрофлоксацин – 6%, офлоксацин – 1%, пефлоксацин – 0,9–2%), главным образом у лиц с судорожной готовностью или как следствие неблагоприятного взаимодействия с другими лекарственными средствами (теофиллин, имипенем, метронидазол, фенбуфен). Механизм этих явлений видится в противодействии ФХ связыванию с рецептором гамма-аминомасляной кислоты [P. Dellamonica, 1996].
Поражение костно-мышечной системы (1%) проявляется в виде миозитов, артралгий, тендопатий с разрывом сухожилий. Эти побочные эффекты носят возраст- и препаратзависимый характер: чаще наблюдаются у пожилых мужчин с дисфункцией почек на фоне одновременного лечения пефлоксацином и глюкокортикостероидами [E. Kentz, 1998].
Безопасность фторхинолонов
По совокупным международным данным (более 10 000 пролеченных детей) профиль безопасности ФХ у детей существенно не отличается от такового у взрослых. Общее число побочных эффектов составило 21,7% [V. Chysky, 1992; R. Kuhn, 1992; M. Schmidt, 1992; U.B. Schaad, 1994]. Все же применение ФХ у детей резко ограничено. Объясняется это возможностью повреждения ФХ суставного хряща, поскольку этот эффект был выявлен у неполовозрелых лабораторных животных (крысы, кролики, собаки) при токсикологических исследованиях.
Хинолоновая артропатия (ХА) развивалась у экспериментальных животных чаще в коленных суставах и клинически выражалась в их припухлости с выпотом невоспалительного характера и хромоте, а также последующем замедлении роста. Макроскопически повреждение суставного хряща проявлялось образованием пузырей, при разрушении которых обнаруживались трещины и эрозии. Микроскопически определялось расщепление и деструкция хрящевой ткани, при этом происходило замещение хрящевой ткани соединительной, т. е. повреждение являлось необратимым. При однотипности макро- и микроскопических проявлений экспериментальная ХА отличалась целым рядом особенностей, обладая видо-, возраст-, и дозозависимым характером.
Наиболее чувствительными к ФХ оказались щенки различных пород собак, причем в определенный возрастной период – от 2 недель до 6 месяцев. Именно у собак артротоксический эффект развивался на дозах ФХ, близких к применяемым в педиатрической практике – 30 мг/кг (10–50 мг/кг), тогда как у крыс, кроликов и свиней – только при использовании доз, значительно (в 15–20 раз) превышающих терапевтические дозы для человека. Мыши и мартышки оказались нечувствительными к артротоксическому действию ФХ. Таким образом, в суставной реакции на ФХ у экспериментальных животных главным является поражение хряща – токсическая хондропатия, а синовиальная оболочка при этом может оставаться интактной или инфильтрироваться мононуклеарами.
Между тем клинические данные расходятся с экспериментальными [О.И. Мохов, 1989; S. Chambers, 1995; И.К. Волков, 2005; E. Kerem, 2005]. Известно, что ХА встречается и у взрослых, хотя и реже, чем у детей: например, на ципрофлоксацин соответственно 0,05–0,6% и 1,3–2,4% [П. Шахт, 1989; I. Simon, 1990]. Эта разница объясняется V. Chysky [1992] несколькими причинами:
а) поводом для назначения ФХ детям являются жизнеугрожаюшие инфекции, требующие более высоких, чем у взрослых (в перерасчете на килограмм массы), доз и большей продолжительности лечения;
б) довольно часто (7–8%) у больных МВ возникают артралгии при применении антибиотиков других классов, например цефалоспоринов, макролидов или аминогликозидов [Безопасность лекарств, 1999; A. Danisovicova, 1995];
в) значительную часть детей (62%), у которых ФХ применяются по жизненным показаниям, составляют больные МВ, страдающие собственной, так называемой муковисцидозной артропатией [D. Schroeder, 1994; M. Hodson and D. Geddes, 1995; C. Hill, 1998; S. Conway, 1998]. МВ-ассоциированные артропатии (МВА) встречаются (8,5%) в любом возрасте, кроме младенческого (средний возраст – 10,5 лет). Им свойственны острое начало (вне связи с обострением бронхолегочного процесса) с вовлечением крупных и средних суставов рук и ног.
Следовательно, артритическая симптоматика связана скорей с природой заболевания, чем с применяемыми препаратами, и поэтому не является строго хинолон-специфической.
Подтверждением этого является тот факт, что общая частота артропатий у детей, за вычетом больных МВ, оказывается близкой к таковой у взрослых – 0,06–0,1%. Известно также, что у 7–8 % больных МВ артралгии возникают при применении антибиотиков других классов, например цефалоспоринов и аминогликозидов [A. Danisovicova, 1995].
Кроме того, ХА в клинической практике отмечается у детей только пубертатного возраста (преимущественно у девочек-подростков), учащаясь к 20 годам [E. Pertuiset, 1989], тогда как в эксперименте – у неполовозрелых животных (у крыс – только у самцов). Необходимо подчеркнуть при этом, что довольно значительный опыт применения ФХ у новорожденных детей (включая недоношенных) и грудных детей при длительности лечения до 49 дней и дозах 15–40 мг/кг/день не выявил у них изменений со стороны костномышечной системы, как этого можно было ожидать, исходя из экспериментальных данных [Н.В. Белобородова, 1996; Е.Н. Падейская, 1998].
К тому же ХА у детей, совпадая с экспериментальной во внешних проявлениях – симметричное, билатеральное поражение прежде всего голеностопных и коленных суставов – не совпадает с ней в главном: эти изменения преходящи, нестойки, полностью разрешаются в сроки от 7 дней до 3 месяцев [R. Javier, 1992], т.е. в отличие от экспериментальной ХА не носят необратимого, инвалидизирующего характера и протекают как острый реактивный артрит.
Есть и еще важное несовпадение – синовиальная жидкость на высоте ХА у детей, будучи стерильной, носила воспалительный характер, что позволило U. Schaad [1992] назвать ХА острым артритом. Многочисленные специальные исследования (прижизненные и посмертные) подтвердили доброкачественный характер ХА у детей.
Методом, который позволяет прижизненно оценить морфологию сустава, является ядерномагнитный резонанс (ЯМР). В исследовании U. Schaad [1998] осуществлялось ЯМР-мониторирование возможного повреждения суставов у 13 детей с МВ (6–13 лет), получавших ципрофлоксацин в дозе 30 мг/кг в 2 приема на протяжении 3 месяцев и не имевших признаков ХА. ЯМР левого коленного сустава проводился до и в конце лечения, а также 4–6 и 15–21 месяц спустя. При этом не было выявлено каких-либо патологических изменений в структурах сустава, а единственной находкой было статистически достоверное утолщение суставного хряща, которое автор объясняет не прямым действием ФХ, а связывает со скачком в росте, наблюдавшимся у детей в результате улучшения состояния на фоне лечения.
В этой же работе проводилось измерение роста у 13 детей (средний возраст 9,5 лет) на основе индивидуального перцентиля в течение 18 и 24 месяцев после применения ФХ. Исследование не выявило отклонений от нормы, что может косвенно свидетельствовать об отсутствии поражения ФХ зоны роста костей. С.Ю. Семыкин (2002) оценивал физическое развитие 78 детей с МВ (1–17 лет), получавших ципрофлоксацин в суточной дозе 15–50 мг/кг в течение 3 и 5 лет, на основе масса-ростового индекса, а также годовую скорость роста. Контрольную группу составили 20 больных МВ (1–15 лет), не получавших ципрофлоксацин. Показано, что параметры физического развития (линейный рост в основной и контрольной группах) достоверно не различались. Этим же автором проводился артрологический осмотр у 78 больных МВ, получавших ципрофлоксацин на протяжении 5 лет. Не было отмечено каких-либо изменений со стороны костномышечной системы. Аналогичные данные о состоянии роста у 40 детей, больных МВ и получавших ципрофлоксацин, были получены итальянскими авторами [L. Romano et al., 2005]. ЯМР-исследование, проведенноена высоте ХА у детей пубертатного возраста [I. Dab, 1992; H. Chung, 1996; A. Wilson, 1997, L. Romano et al., 2005], выявило у них только одно отклонение от нормы – cиновит (выпот и утолщение синовиальной оболочки). Прямой ответ на вопрос о возможности повреждения ФХ покровного хряща у детей могли бы дать только морфологические исследования. Обстоятельное морфологическое исследование провел С.Ю. Семыкин и С.С. Постников (2002), осуществив макро- и микроскопическое, а также морфометрическое изучение структур коленного сустава (морфолог В.П. Нажимов) у 11 больных МВ в возрасте от 4 до 16 лет, не имевших при жизни проявлений ХА. Общая продолжительность применения ципрофлоксацина в суточной дозе 15–50 мг/кг составила 216 дней. Контрольную группу составили 10 практически здоровых детей, погибших в результате автотравмы. Было показано, что макроскопическая картина суставного хряща и зоны роста не отличаются от таковой у практически здоровых детей. Автор подчеркивает, что при макро- и микроскопическом сравнении аналогичных участков покровного хряща у больных, получавших один или несколько курсов ципрофлоксацина, у детей дошкольного и школьного возраста различий не было выявлено, т.е. вне зависимости от возраста ребенка и длительности применения ципрофлоксацина риска хондротоксичности у ФХ нет. Автор отметил и другое: 8 из 11 больных МВ умерли в результате далеко зашедшего легочного процесса на фоне очередного применения ципрофлоксацина или пефлоксацина, как последнего средства надежды; тем самым морфологически у этих больных оценивался как будто острый и отсроченный (с учетом прежнего применения ФХ) возможный хондротоксический эффект ФХ одновременно. Но никаких изменений в суставном хряще не было выявлено. Зона роста во всех случаях оставалась интактной. Таким образом, вопрос о широком применении ФХ у детей остается на сегодняшний момент дискутабельным. В работах, приведенных в данной статье, показано, что ФХ, являясь хондротоксическими у многих неполовозрелых лабораторных животных, не оказывают подобного эффекта у детей ни при однократном, ни при повторном применении.
Список использованной литературы находится в редакции.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник

Дорогие фармтруженики, здравствуйте!
Недавно мы с вами разбирали наиболее популярные группы антибиотиков.
Сегодня я бы хотела остановиться еще на одной группе чрезвычайно популярных антибактериальных средств. Я говорю о фторхинолонах.
Они не являются антибиотиками, поскольку не имеют природных аналогов. Но по эффективности ничуть им не уступают.
Вы можете не читать дальше, если быстро ответите на вопросы:
- Сколько поколений фторхинолонов сейчас существует на рынке?
- Назовите хотя бы по одному препарату каждого поколения этой группы.
- Чем поколения отличаются друг от друга?
- Какие из фторхинолонов применяются, преимущественно, при инфекциях мочеполовой системы?
- Назовите редкий побочный эффект, который вызывают препараты этой группы.
- С какого возраста можно применять фторхинолоны и почему?
Ну как? Справились?
Если не очень, продолжаем разговор.
Из истории фторхинолонов
«Родителями» фторхинолонов являются хинолоны – налидиксовая кислота (Неграм, Невиграмон), пипемидовая кислота (Палин) и др.
Я уверена, вы с лёту назовете, когда они используются.
Назвали?
Правильно. Преимущественно, при инфекциях мочевыводящих путей. Хинолоны — это по сути уросептики, т.е. препараты, освобождающие от бактериальных оккупантов мочевой пузырь, почки, мочеточники.
В последнее время эти средства назначаются все реже и реже, поскольку на рынке появились куда более эффективные препараты.
Хинолоны были синтезированы случайно, во время изучения антималярийного средства под названием Хлорохин.
Через несколько лет после их открытия кому-то из ученых пришла в голову идея присоединить атом фтора к формуле хинолонов и посмотреть, что из этого получится. А получилась совершенно новая группа антибактериальных средств, которая по эффективности сравнима с цефалоспоринами.
Группа фторхинолонов. Особенности поколений
В некоторых публикациях хинолоны рассматриваются вместе с фторхинолонами и причисляются к их первому поколению.
Белиберда какая-то получается: хинолоны являются 1 поколением ФТОРхинолонов.
Но группа-то получилась совсем другая, с иными характеристиками и показаниями!
Так что я буду говорить, как подсказывает мне здравый смысл.
На сегодняшний день существует 3 поколения фторхинолонов:
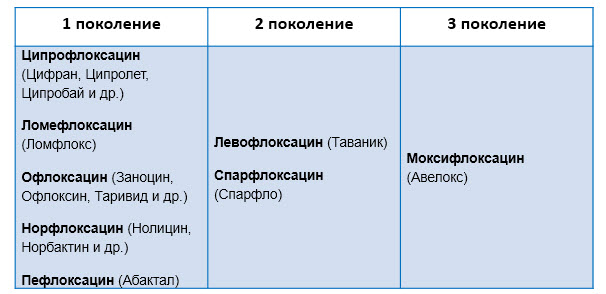
Поколения фторхинолонов отличаются друг от друга спектром антибактериальной активности.
Каждое новое поколение в чем-то превосходит предыдущее.
1 поколение называют «грамотрицательным», поскольку препараты, относящиеся к этому поколению, действуют на широкий спектр грамотрицательных бактерий. А из грамположительных лишь на небольшую кучку: несколько разновидностей стафилококка, листерии, коринебактерии., туберкулезную палочку.
Напомню вам грамотрицательные бактерии: синегнойная палочка, гонококк (возбудитель гонореи), менингококк (возбудитель гнойного менингита), кишечная палочка, сальмонелла, шигелла, протей, клебсиелла, энтеробактер, гемофильная палочка и др.
Препараты 1 поколения можно разделить на 2 группы:
Системные: Ципрофлоксацин, Ломефлоксацин и Офлоксацин. Они проникают в различные органы и ткани, поэтому используются при инфекциях самых разных локализаций: дыхательных путей, уха, глаза, придаточных пазух носа, мочеполовой сферы, ЖКТ, кожи, костей и др.
Уросептики: Норфлоксацин и Пефлоксацин. Эти средства создают высокие концентрации в моче, поэтому применяются чаще всего при инфекциях мочеполовой системы.
Но препараты этого поколения слабо действуют на пневмококк, хламидии, микоплазмы, анаэробы.
Норфлоксацин также входит в состав глазных и ушных капель под названием Нормакс.
2 поколение получило название «респираторного», так как относящиеся к нему средства действуют не только на тех возбудителей, что и 1 поколение, но и на большинство возбудителей инфекций дыхательных путей (пневмококк, Mycoplasma pneumoniae и др.).
Они отлично расправляются с теми же врагами народа, что и 1 поколение, но еще с пневмококками, хламидиями, микоплазмами.
3 поколение я назову «гроза анаэробов».

Пока собирала материал для статьи, встречала несколько представителей этого поколения, но не увидела их в ассортименте аптек. О «мертвых душах» говорить не вижу смысла. Так что называю самый популярный: Моксифлоксацин (торговое название Авелокс).
Препараты, вернее, препарат, третьего поколения фторхинолонов действует на тех же возбудителей, что и два предыдущих, плюс способен уничтожать анаэробные бактерии. Помните, кто это такие?
Это неприхотливые микробы, которым, в отличие от своих братьев по разуму, для полноценной жизни не нужен кислород.
Они вызывают тяжелейшие инфекции. Их токсины чрезвычайно агрессивны, способны поражать жизненно важные органы и вызывать перитонит, абсцессы внутренних органов, сепсис, остеомиелит и другие серьезные болячки.
Анаэробные бактерии являются также виновниками столбняка, газовой гангрены, ботулизма, пищевых токсикоинфекций.
Таким образом, от поколения к поколению спектр антибактериальной активности фторхинолонов расширяется.
Преимущества группы фторохинолонов
Вы, наверное, заметили, что препараты этой группы полюбились многим врачам, поэтому назначают их довольно часто.
Что же хорошего они в них нашли?
Давайте перечислим их преимущества.
Фторхинолоны:
- Имеют широкий спектр действия.
- Глубоко проникают в различные ткани.
- Имеют длительный период полувыведения, поэтому могут применяться 1-2 раза в сутки.
- Хорошо всасываются в желудочно-кишечном тракте, поэтому выпускаются в виде пероральных форм, что для многих больных удобнее и приятнее.
- Высоко эффективны.
- Хорошо переносятся.
Механизм действия фторхинолонов
Фторхинолоны оказывают бактерицидное действие. Они подавляют ферменты, которые необходимы для синтеза ДНК дочерних бактериальных клеток. А что такое ДНК? Это «сердце» клетки, ее генетический код, «инструкция», как ей жить-поживать и добра наживать. Нет «инструкции» – нет и жизни.
Показания к применению фторхинолонов
Фторхинолоны имеют широкий, я бы даже сказала, широчайший, круг показаний:
- Заболевания верхних и нижних дыхательных путей.
- Инфекции мочевыводящих путей и предстательной железы: цистит, уретрит, пиелонефрит, простатит. Особенно хорошо с ними справляются норфлоксацин и пефлоксацин.
- Гонорея, хламидиоз, микоплазмоз.
- Интраабдоминальные инфекции (перитонит, холецистит и др.).
- Кишечные инфекции (сальмонеллез, дизентерия, холера и пр.).
- Инфекции кожи, мягких тканей, костей и суставов.
- Сепсис.
- Менингит.
- Туберкулез.
- Инфекции глаз, наружного уха (норфлоксацин).
Выбор препарата группы фторхинолонов зависит от вида и тяжести заболевания, его длительности, вида возбудителя и эффективности используемых ранее препаратов.
Каждый препарат имеет свои преимущества. Например:
Ципрофлоксацин – наиболее активный из фторхинолонов в отношении грамотрицательных бактерий. Превосходит своих «коллег» по действию на синегнойную палочку. Применяется в комбинированной терапии лекарственноустойчивых форм туберкулеза.
Офлоксацин — из 1 поколения самый активный в отношении пневмококков и хламидий, но слабее препаратов 2 и 3 поколений.
Норфлоксацин и пефлоксацин особенно хороши при инфекциях мочевыводящих путей и простаты.
Пефлоксацин, помимо этого, лучше других фторхинолонов проникает через гематоэнцефалический барьер, поэтому используется при менингитах (для этого есть форма концентрата для в/в введения).
Спарфлоксацин превосходит другие препараты этой группы по длительности действия. Применяется однократно в сутки.
Левофлоксацин — изомер офлоксацина, в 2 раза активнее его и лучше переносится.
Моксифлоксацин из всей группы самый активный в отношении пневмококков, хламидий, микоплазм, анаэробов. Может применяться эмпирически (то есть вслепую, без высева бактерий) при тяжелых инфекциях различных локализаций.
Противопоказания к применению фторхинолонов
Общие для всех:
- Беременность.
- Кормление грудью.
- Аллергические реакции на фторхинолоны.
- Детский и подростковый возраст.
Фторхинолоны противопоказаны до 18 лет, так как в опытах на животных исследователи отметили задержку развития хрящевой ткани. Поэтому их, как правило, не назначают до окончания формирования скелета. Хотя, в ряде случаев, врачи под свою ответственность назначают детям фторхинолоны. Например, при муковисцидозе или непереносимости других антибактериальных средств.
Наиболее частые побочные эффекты фторхинолонов
- Со стороны ЖКТ: боли в животе, тошнота, рвота, диарея. Поэтому советуйте их принимать после еды.
- Нарушения со стороны ЦНС: головная боль, головокружение, судороги (у людей, страдающих эпилепсией).
- Фотодерматозы, т.е. повышенная чувствительность кожи к ультрафиолетовым лучам. Под действием солнца фторхинолоны разрушаются, образуются свободные радикалы и вызывают повреждение кожи.
А значит, при продаже препарата из этой группы нужно предложить солнцезащитное средство. Особенно летом и в солнечных регионах.
Больше других способностью вызывать фотодерматозы отличаются ломефлоксацин (Ломфлокс) и спарфлоксацин (Спарфло).
- Повышение печеночных трансаминаз. Это означает, что препараты гепатотоксичны. Поэтому неплохо бы средство из группы фторхинолонов принимать в связке с гепатопротектором. Редко, но случается лекарственный гепатит.
- Увеличение интервала QT на ЭКГ. Для здоровых людей это не страшно. А если препарат принимает человек, имеющий серьезные проблемы с сердцем, может быть аритмия. Но это случается при приеме больших доз препарата.
- Редкое побочное действие – тендинит, т.е. воспаление сухожилия, и его разрыв. Чаще всего, страдает ахиллово сухожилие. Это бывает, преимущественно, у пожилых людей.
Тендиниты возникают потому, что фторхинолоны подавляют активность фермента, необходимого для синтеза белка коллагена. А он составляет основу сухожилий, да и вообще соединительной ткани.
Важно:
Если фторхинолоны принимать одновременно с антацидом и витаминно-минеральным комплексом, образуются нерастворимые соединения, и препарат должного эффекта не окажет. Поэтому перерыв между их приемами должен составлять не менее 4 часов.
А теперь вспомним все выше сказанное и набросаем список рекомендаций покупателю.
5 рекомендаций покупателю при продаже препарата группы фторхинолонов
Если вы продаете препарат из группы фторхинолонов:
- Предложите солнцезащитное средство. Говорите примерно так: «Этот препарат повышает чувствительность кожи к солнечным лучам и может вызвать появление сыпи. Поэтому я Вам советую приобрести еще средство для защиты кожи от солнца».
- Если человек отказывается от пункта 1, предупредите: «Избегайте пребывания на солнце весь период лечения и еще 3 дня после его окончания».
- Предложите гепатопротектор («С этим препаратом Вам врач выписал что-нибудь для защиты печени?»)
- Скажите, что принимать средство нужно после еды, запивать большим количеством жидкости, чтобы уменьшить его раздражающее действие на желудок.
- Если человек вместе с препаратом группы фторхинолонов приобретает еще антацидный препарат или витаминно-минеральный комплекс, порекомендуйте развести их прием во времени (перерыв не менее 4 часов).
На сегодня все. Как вам понравилась статья, друзья?
Все ли понятно?
Если есть, что добавить, прокомментировать, пишите в окошечке комментариев ниже.
Буду признательна, если вы поделитесь ссылкой на статью со своими коллегами.
До новой встречи на блоге «Аптека для человека»!
С любовью к вам, Марина Кузнецова
P.S. Если Вы еще не подписаны на новые статьи блога, Вы можете сделать это прямо сейчас, потратив всего несколько минут. Для этого нужно заполнить форму подписки, которую Вы видите в конце каждой статьи и справа в верхней части страницы. Не забудьте подтвердить подписку в пришедшем письме. После этого Вы получите письмо со ссылкой на скачивание полезных шпаргалок.
Если не получили письмо, проверьте папку «спам».
Что-то пошло не так? Посмотрите инструкцию.
Все равно не получилось? Пишите. Разберемся!
Источник
