Лимфома и побочные действия

Химиотерапия при лимфоме — это спасение жизни, которую иными способами сохранить не удастся. Конечно лекарства не обещают 100% радикальности, как операция при раке, но вместе с облучением это единственно возможное и эффективное лечение. Проблема в том, что лимфомы способны изменяться, что обещает рецидивы и независимость от терапии.
Как проходит химиотерапия при лимфоме
При подавляющем большинстве злокачественных лимфом или лимфосарком химиотерапия подаётся на первое-второе и на третье, при некоторых клеточных вариантах после первой линии дополняется лучевой терапией в скромных, по сравнению с раковыми заболеваниями, дозах.
Роль облучения — поддержка достигнутого результата и дополнение его позитивом. Сегодня полностью отошли от радикальной программы лучевой терапии, несколько десятилетий доминировавшей при лимфоме Ходжкина, отказавшись от профилактического облучения не поражённых опухоль лимфоколлекторов. Из профилактического — только введение цитостатиков в спинномозговую жидкость, уменьшающее вероятность злокачественного поражения головного мозга и его оболочек.
Химиотерапия злокачественных лимфом получила новое развитие, наряду с проверенными десятилетиями схемами в «золотой стандарт» включена высокодозная ХТ (ВДХТ) с обязательной пересадкой предварительно собранных собственных кроветворных клеток. Пока не удалось разрешить трагическую дилемму трансплантации — она помогает пациенту выжить, но может способствовать рецидиву.
Сегодняшнее противоопухолевое лечение лимфом отобрало самые результативные комбинации, учитывающие иммуногистохимические характеристики злокачественных клеток. Для каждого прогностического варианта определено оптимальное число циклов, возраст больного и его хронические болезни уже не противопоказание для активного лечения, потому что созданы лекарственные комбинации на все случаи болезни, тем не менее, ограничения по применению цитостатиков включены в стандарты.
Химиотерапия используется всегда, когда в ней есть необходимость и нет абсолютных противопоказаний. На выборе схемы лечения сказываются не только клеточный вариант и прогностические характеристики лимфомы, распространённость болезни по данным ПЭТ-КТ, но и исходное состояние здоровья пациента.
Химиотерапия при лимфоме Ходжкина
Лимфома Ходжкина (или по-старому лимфогранулематоз) — одно из самых благоприятно текущих заболеваний лимфоидной ткани. Ходжкинская лимфома входит в ограниченное число болезней, излечиваемых только одной химиотерапией, но важная ремарка: диагностированная на ранней стадии и с признаками благоприятного течения. Прогноз ожидается малооблачным при небольшом поражении — не более двух групп лимфоузлов в верхней или нижней половине тела — по одну сторону диафрагмы, лучше без вовлечения лимфоузлов средостения и с исходными нормальными клиническими и биохимическими анализами крови.
Каждого пациента после первичного обследования относят к трём основным группам, по стандартам которых будет проводится противоопухолевое лечение, во всех случаях на первом этапе проводится химиотерапия, затем результат закрепляется трёхнедельным облучением зон поражения.
Первичная терапия из четырёх цитостатиков и «золотой стандарт» — схема ABVD, но при неважном прогнозе на излечение молодым пациентам (а молодые — это граждане до 50 лет без хронических болезней) может предлагаться терапия шестью и даже восемью препаратами, что при снижении частоты неудач терапии повышает трёхлетнюю выживаемость. Многокомпонентные комбинации чреваты 100% повреждением форменных элементов крови, поэтому в схему часто входит стимуляция выработки лейкоцитов (нейтрофилов).
Число курсов зависит от исходного поражения и прогноза, в лучшем случае при лимфоме I-II стадии предложат от 2 до 4 циклов четырёхкомпонентной схемы. При том же объёме поражения, но худших прогностических факторах, потребуется 4-6 курсов. Для повышения результативности первых два цикла у сохранных молодых пациентов заменяют на 6-компонентную схему, затем проводят 2 стандартных ABVD и можно уходить на облучение.
Распространенные стадии не обещают хорошего прогноза, поэтому химиотерапия длительная и многокомпонентная. Причём сколько циклов потребуется — 6 или 8, определят по результатам первых 4 циклов: если опухоль полностью ушла и ПЭТ это покажет — предложат пройти только два цикла, затем назначается трёх-четырёхнедельное облучение. При незначительном эффекте — 8 циклов и лучевая терапия на пораженные лимфоузлы.
Высокодозная химиотерапия с трансплантацией гемопоэтических, то есть кроветворных костномозговых, стволовых клеток проводится при рецидиве лимфомы Ходжкина. Для подготовки к высокодозному лечению за 2 недели введут винбластин или винкристин, так называемую терапию «спасения», что позволит определиться со степенью реакции на цитостатики, уменьшить объем поражения лимфоузлов, а также предотвратить очень опасную реакцию массивного распада опухолевых узлов.
У пожилых пациентов, в популяции это каждый третий больной, лечение выбирается с учетом хронической патологии. Так у курильщиков и страдающих болезнями легких в комбинацию не включают блеомицетин, накапливающийся в легочной ткани и вызывающий специфическое воспаление. При сердечной патологии кардиотоксичные антрациклины заменяют на другие противоопухолевые антибиотики.
Лимфома Ходжкина чувствительна к множеству цитостатиков, что позволяет найти оптимальную комбинацию, вплоть до применения одного-единственного цитостатика.
Химиотерапия при неходжкинских лимфомах
Неходжкинские лимфомы представлены множеством морфологических видов, каждый с особенностями течения и лечения. Разберём самые частые варианты заболевания.
Самая благоприятная по течению фолликулярная лимфома встречается в каждом пятом случае злокачественных лимфом у взрослых. В самом начале процесса без явных признаков активности не всегда требуется безотлагательная химиотерапия, у некоторых пациентов прогноз настолько неплох, что можно ограничиться облучением лимфомы либо длительным наблюдением с тщательным мониторингом анализов и регулярным обследованием каждые 3 месяца.
Сразу ХТ начинается только при вовлечении в злокачественный процесс любых органов или при поражении не менее трёх лимфатических зон с размером узлов более 3 сантиметров, или при лихорадке с потливостью, или при плохих показателях крови.
Оптимальный режим — R-CHOP, сочетающий сравнительно мягкие в плане осложнений алкилирующие цитостатики с иммунным препаратом ритуксимабом. Это моноклональное антитело при начальном и прогностически благоприятном процессе используют без ХТ — в монорежиме внутривенно, подкожно каждые 8 недель в течение двух лет применяют для поддержания позитивного результата после завершения циклов.
Вопрос о высокодозной химиотерапии с пересадкой костного мозга ставится при рецидиве или переходе фолликулярной лимфомы в более агрессивную, вероятность чего возрастает с течением времени, так через 10 лет переход в диффузную В-крупноклеточную лимфому отмечается у каждого шестого, а через 15 лет — у каждого второго. По истечении полутора десятилетий после первичного лечения частота рецидивов лимфомы сходит на нет.
У каждого третьего первичного пациента с лимфомой выявляют диффузную крупноклеточную В-клеточную лимфому (ДВКЛ), ежегодно её диагностируют только у пяти из каждых ста тысяч россиян.
Стандарт химиотерапии при неагрессивном варианте ДВКЛ, позволяющий 80% больных прожить дольше пятилетки — 6 циклов комбинации CHOP с ритуксимабом. При полном уничтожении новообразований в результате лекарственного воздействия, возможно подключение лучевой терапии в обычной для лимфом дозе 30-36 грей, а при остаточных опухолевых очагах дозу облучения доводят до 36-40 Грей.
Аналогичная комбинация цитостатиков с иммунным препаратом неважно работает при агрессивном варианте и большом распространении, поэтому химиотерапию усугубляют уменьшением интервалов между циклами R-CHOP или переводят на многокомпонентные комбинации.
При неблагоприятном прогнозе всем пациентам уже на первой линии проводится профилактика поражения головного мозга — введение высоких дох метотрексата и цитарабина в спинномозговую жидкость.
После завершения основной программы поддерживающая химиотерапия не проводится из-за не столь хорошей чувствительности опухолевых клеток к лекарствам. При рецидиве крупноклеточной лимфомы прибегают к комбинациям 2-й линии и трансплантации стволовых клеток крови после высокодозной ХТ.
Периферическая Т-клеточная лимфома — каждый четвёртый случай злокачественного поражения Т-клеточного ростка кроветворения или каждая шестая лимфома. Морфологически группа представлена разнообразными клеточными вариантами. Агрессивно текущее заболевание, как правило, вовлекает не только лимфатические узлы, но и другие органы.
В первой линии используют традиционный CHOP, но в редких случаях удается отказаться от ВДХТ с аутологичной трансплантацией клеток костного мозга. Некоторые виды лимфом благоприятного течения отзываются на облучение и L-аспарагиназу. При отсутствии эффекта лечение подбирается индивидуально.
Лимфомы одного названия предполагают множество различных морфологических вариантов заболевания, внутри групп клетки различаются ИГХ-характеристиками, предполагающими возможности индивидуального подбора противоопухолевого лечения, поэтому специалисты нашей Клиники могут предложить не один-два стандарта, а десятки комбинаций ХТ.
Возможные осложнения после химиотерапии при лимфоме
Тошноту и рвоту уменьшает включение в схемы глюкокортикоидных гормонов. Многокомпонентные комбинации обязательно предваряются введением антиэметиков, приём которых продолжается после завершения терапии.
Для профилактики нейтропении через сутки после цитостатика вводят стимулятор КСФ, что помогает не снижать следующую дозу и не увеличивать интервал без лечения.
Повреждение миокарда характерно для антрациклинов, облучение средостения дополнительно увеличивает кардиотоксичность. Осложнение может проявиться через несколько лет, профилактика не разработана, поэтому у страдающих сердечно-сосудистыми болезнями из схемы исключают антрациклины.
При чувствительности к ХТ и большом распространении лимфомы возможно развитие синдрома лизиса опухоли (СЛО), когда вышедшие из погибшие опухолевых клеток вещества отравляют организм, приводя к почечной недостаточности и гиперкалиемии с фатальной аритмией. Индуцированный лекарствами распад опухоли научились предотвращать.
При пересадке донорского костного мозга высока вероятность отторжения — реакция трансплантат-против-хозяина. При высокодозной терапии отдается предпочтение пересадке собственных клеток даже при угрозе рецидива лимфомы. Рецидив можно вылечить, отторжение трансплантата фатально для пациента.
Методы химиотерапии при лимфоме
Пациент получает лечение всеми способами, кроме внутримышечных инъекций из-за раздражающего действия цитостатиков и опасности осложнений со стороны мягких тканей.
Большинство цитостатиков вводится внутривенно струйно — болюсно или капельно.
Частый компонент схем — преднизолон принимается в таблетках, цитостатик прокарбазин — в капсулах.

Ритуксимаб применяется внутривенно и подкожно, подкожные инъекции удобны для поддержки.
Профилактика нейролейкемии проводится интратекально — введением препарата в спинномозговой канал, потому что организм специальным гематоэнцефалическим барьером защищает головной мозг от проникновения лекарства в крови.
Противопоказания к применению химиотерапии при лимфоме
Абсолютные противопоказания к ХТ при лимфомах — только декомпенсация других хронических заболеваний с существенным снижением функции органов.
Лимфомы чувствительны к лекарствам, а эффективное лечение существенно улучшает состояние, поэтому к терапии прибегают и у тяжелых больных с прогрессированием злокачественного процесса.
При ограниченных физических возможностях пожилых пациентов с большим числом хронических болезней подбирают «посильную» терапию, благо спектр активных препаратов при лимфоме очень объемен.
Препараты, применяемые при химиотерапии
При лимфомах применяется почти два с половиной десятка противоопухолевых препаратов, из которых составляют несколько десятков схем. Можно пересчитать по пальцам цитостатики, не используемые при лимфосаркомах.
Рацион и диета при химиотерапии при лимфоме
Из-за морфологической разнородности и множества клинических вариаций лимфом не было ни одного клинического исследования по симптоматической и сопроводительной терапии.
Диета должна учитывать исходное состояние организма и понесенные им в результате ХТ потери, поэтому общих рекомендаций «для всех» не существует, подбор оптимального питания всегда индивидуален и должен осуществляться специалистом-нутрициологом.
Прогнозы для пациентов
Эффективность лечения оценивают в середине программы и по её окончании, причём оптимально ПЭТ-КТ обследование.
На прогнозе сказывается очень много факторов, для каждого заболевания разработан свой прогностический индекс, поэтому и в диагнозе обязательно указывают прогностическую группу.
В конечном итоге перспективы на дальнейшую жизнь определяет результат химиотерапии и скорость развития рецидива.
Каждому хочется знать — что ждёт впереди, при злокачественном процессе важнее — как лечат и где лечат, потому что без современного обследования невозможно подобрать оптимальную терапию. В Европейской клинике всё проходит на очень высоком уровне, вы можете лично убедиться в этом.
Список литературы:
- Демина Е.А., Тумян Г.С., Унукова Е.Н., и соавт./ Современные возможности лечения первичных больных лимфомой Ходжкина и причины неудач лечения// Онкогематология; 2007; 2.
- Нестерова Е.С., Кравченко С.К., Гемджян Э.Г., и соавт./ Итоги десятилетного опыта лечения больных фолликулярной лимфомой// Гематология и трансфузиология; 2012; 57(5).
- Ткачев С.И., Демина Е.А., Трофимова О.П., Сахаровская В.Г./ Современное лечение больных с ранними стадиями лимфомы Ходжкина// Вопросы онкологии; 2007;53(1).
- Engert A., Plutschow A., Eich H.T., et al. /Reduced treatment intensity in patients with early-stage Hodgkin’s lymphoma//N Engl J Med; 2010; 363.
- Jagadeesh D., Diefenbach C., Evens A. /Hodgkin lymphoma in older patients: challenges and opportunities to improve outcomes// Hemat Oncol; 2013; 31(suppl. 1)
- Cheson B.D., Pfistner B., Juweid V.E., et al. /Revised Response Criteria for Malignant Lymphoma// JCO; 2007; 25.
- Swerdlow A.J., Higgins C.D., Smith P., et al./ Second cancer risk after chemotherapy for Hodgkin”s lymphoma: a collaborative British cohort study// J Clin Oncol; 2011; 29.
Источник
Дата публикации 29 мая 2020Обновлено 29 мая 2020
Определение болезни. Причины заболевания
Лимфомы — это заболевания, для которых характерен первичный локальный злокачественный опухолевый рост, исходящий преимущественно из внекостномозговой лимфоидной ткани. В отличие от лейкозов с первичным поражением костного мозга и лейкемическими нарушениями периферической крови, лимфомы локализуются в лимфатических узлах, в той или иной степени проникая в окружающие ткани. При этом в костном мозге долгое время опухолевые клетки не образуются.
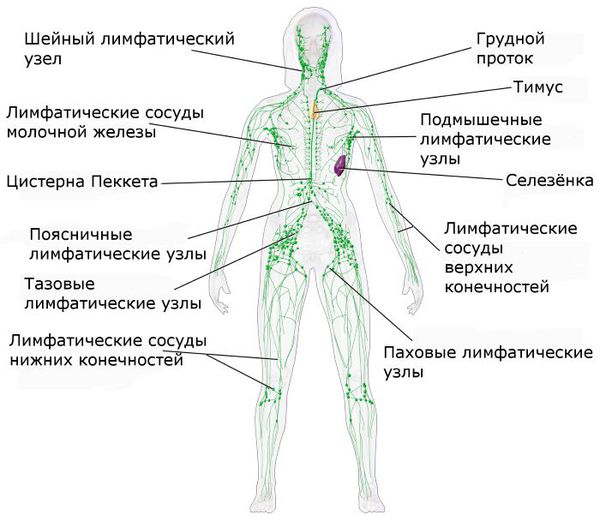
Лимфомы подразделяются на две большие группы: лимфогранулематоз (болезнь Ходжкина или ходжинские лимфомы) и неходжкинские лимфомы (лимфосаркомы, НХЛ) [1]. Ходжкинские лимфомы встречаются в 40 % случаев, а неходжкинские — в 60 %. Единственный достоверный дифференциальный признак ходжкинских лимфом в отличие от неходжкинских — морфологическое исследование, при котором находят специфические для болезни Ходжкина клетки Березовского — Штернберга — Рида. В дальнейшем для уточнения диагноза проводят иммуногистохимическое исследование.
В структуре онкологических заболеваний Российской Федерации лимфома Ходжкина занимает 9-10 место. Мужчины болеют чаще женщин, городские жители — чаще сельских.
Отмечено два пика заболеваемость лимфомой Ходжкина у взрослых:
- Возраст 20-30 лет.
- Старше 60 лет.
Вероятно, первый пик связан с пролиферативным потенциалом клеток (способностью к размножению), а второй пик — с ослаблением иммунного контроля.
По данным Российского онкологического центра им. Н. Н. Блохина, в Российской Федерации каждый год выявляются около 10-12 тыс. новых случаев неходжкинской лимфомы, что составляет 2,6 % от всех злокачественных опухолей. Пик заболеваемости приходится на возрастную группу 16-34 лет [2][3].
Этиология лимфом до конца не изучена, существуют особенности течения заболевания у детей и на фоне иммунодефицита (например ВИЧ).
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением – это опасно для вашего здоровья!
Симптомы лимфомы
Первые симптомы заболевания:
- слабость;
- повышение температуры до 38°С и выше;
- потливость, особенно в ночное время.
Первые признаки заболевания совпадают с клинической картиной ОРВИ или ОРЗ.
В течение нескольких недель происходят следующие изменения:
- снижается вес;
- увеличиваются лимфатические узлы.
Нужно помнить о том, что лимфатические узлы могут увеличиваться и при ОРВИ, поэтому не следует излишне паниковать по этому поводу. При увеличении шейных лимфатических узлов необходимо исключить, помимо системных инфекционных заболеваний, патологию зубов, ротоглотки и гортани [3][4]. Лимфатические узлы могут увеличиваться от расчёсов на голове при нервно-аллергических реакциях и педикулёзе, и внесение инфекции через эти расчёсы.
Как правило, увеличенные лимфатические узлы воспалительного характера болезненные при пальпации, плотно-эластичные, часто спаянные с гиперемированной кожей. Напротив, лимфоузлы при лимфоме плотные и абсолютно безболезненные.
Одним из отличительных признаков лимфом является усиление и/или появление боли в лимфатических узлах при употреблении алкоголя. Возникает кожный беспричинный зуд и гиперергическая реакция на укус насекомых (комаров и др.), которой раньше не было [5][8]. При этом необходимо помнить о такой патологии, как болезнь кошачьих царапин — воспалении лимфатических узлов после царапины или укуса кошки в течении 3-25 дней.
При онкологическом заболевании увеличенный лимфатический узел может быть проявлением метастаза. Учитывая, что лимфатический узел является фильтром, который “вылавливает” инфекцию или опухолевую клетку, его увеличение сигнализирует о присутствии патологии и требует внимательного отношения со стороны больного. Изначально может увеличиваться один лимфатический узел и группа регионарных, но может и присутствовать и генерализованное увеличение лимфатических узлов.

В дальнейшем при разрастании опухолевых масс в средостении (части грудной полости, ограниченной спереди грудиной, сзади позвоночником) и компрессии пищевода и верхних дыхательных путей появляется затруднённость дыхания и глотания. При сдавлении сосудистого пучка возникает симптом верхней полой вены, проявляющийся в набухании вен верхних конечностей и особенно головы и шеи [4][5].
Обширное разрастание опухоли в забрюшинном пространстве и брыжейке кишки приводит к кишечной непроходимости, отсутствию мочи с развитием гидронефроза. Соответственно локализация опухолевых клеток в селезёнке приведёт к увеличение селезёнки в размерах и боли в левом подреберье за счёт перерастяжения капсулы селезёнки.
Патогенез лимфомы
Патогенез лимфомы Ходжкина и неходжкинских лимфом различный. При лимфоме Ходжкина лимфоидное новообразование появляется в одном лимфатическом узле или в цепочке лимфоузлов и изначально распространяется в пределах смежных лимфатических узлов. Неходжкинские лимфомы, как правило, возникают вне узлов и распространяются непредсказуемым образом.
Патогенез лимфомы Ходжкина. Выдвигаются различные теории, основные из них:
- генетическая — заболевание возникает при нарушении определённых цепей в генотипе клеток, наблюдается семейная наследственность;
- постинфекционная — в ряде случаев в анамнезе отмечаются перенесённые инфекции, такие как инфекционный мононуклеоз, цитомегаловирус и др.;
- спонтанная бласттраснформация лимфоцитов — превращение лимфоцитов под влиянием различных стимуляторов, в том числе чужеродных антигенов, в бластоподобные формы, способные к делению [3][7].
Патогенез неходжкинской лимфомы. Доказанной теории возникновения НХЛ нет. Отмечается повышенное число заболевших среди следующих пациентов:
- с отягощённой наследственностью, у родственников которых выявлены опухолевые заболевания крови;
- перенёсших инфекционные заболевания;
- после иммуносупрессии и трансплантации печени, почек и сердца [8][9].
Таким образом, лимфомы возникают после сильной встряски иммунной системы с последующим её дисбалансом в виде бласттрансформации. При бласттрансформации по неизвестным причинам не происходит трансформация клеток во взрослый фенотип. Это приводит к большому неконтролируемому образованию бластов, что и является началом опухолевого роста.
Классификация и стадии развития лимфомы
В соответствии с классификацией Ann Arbor (модификация Cotswold) выделяют четыре стадии развития лимфомы [4][5][9].

Стадия I. Характеризуется поражением опухолевыми клетками лимфатических узлов одного региона (регионарное поражение). Допускается поражение одного лимфатического узла из другой регионарной группы, тогда к стадии I добавляется литера “Е”.
Стадия II. Для второй стадии характерно поражение не менее двух лимфатических зон выше или ниже диафрагмы — это могут быть поражённые лимфатические узлы разных регионов, например шейных и подмышечных, узлов средостения и шейных и т. д. Добавление в классификации литеры “Е” происходит при поражении экстралимфатических тканей (печени, селезёнки, костного мозга) и/или органа по ту же сторону диафрагмы.
Стадия III. Поражение лимфатических узлов по обе стороны диафрагмы, например паховых и шейных, паховых и лимфатических узлов средостения. Номенклатура опухоли подразумевает чёткое определение экстранодальных поражений (поражение опухолевыми клетками вне лимфатических узлов):
- III S(1) стадия — с вовлечением селезёнки;
- III E(2) стадия — с локализованным экстранодальным поражением;
- III SE стадия: сочетание III S и III E.
Стадия IV. Множественное поражение лимфатических узлов в различных зонах организма человека или поражение экстралимфатических органов (одного или несколько). При этом лимфатические узлы могут быть как поражены, так нет.
Обязательным в классификации является оценка общего состояния пациента:
- литера “А” добавляется при отсутствии общих симптомов интоксикации;
- литера “В” характеризуется лихорадкой не менее трёх дней подряд выше 38°С, ночной обильной потливостью, снижением веса на 10 % тела за последние 6 месяцев; к “Б” также относятся повышение в крови СОЭ (скорости оседания эритроцитов), церулоплазмина, α2-глобулина, фибриногена, ЛДГ (лактатдегидрогеназы).
- литера “Х” добавляется при значительных размерах опухоли (более 10 см) и при огромных размерах опухолевых масс в средостении.
Осложнения лимфомы
При лимфоме важно оценить общее состояние больного, для этого используется шкала ECOG (Eastern Cooperative Oncology Group) [5][8][9].
| Статус | Определение |
|---|---|
| Физическая активность больного не отличается от активности до заболевания, пациент ведёт себя как абсолютно здоровый человек | |
| 1 | Физическая активность снижена, но пациент сам передвигается и в состоянии выполнять не интенсивные физические нагрузки и заниматься лёгкими видами физической работы и умственным трудом |
| 2 | Физическая активность снижена, появляется утомляемость, но пациент способен самостоятельно передвигаться и обслуживать себя. Усталость компенсируется постельным режимом, которое занимает не более половины светлого времени суток |
| 3 | Физическая активность значительно снижена, пациент не способен полностью обслуживать себя в домашних условиях. Утомляемость вынуждает пациента более половины суток проводить в постели |
| 4 | Самая тяжёлая категория больных, они полностью обездвижены и постоянно находятся в постели или в сидячем положении, не могут себя обслуживать. Минимальная физическая нагрузка моментально истощает их, с пациентами невозможна длительная продуктивная коммуникация |
Осложнения при лимфоме Ходжкина:
- обструкции мочевыводящих путей, пищеварительной и дыхательной систем, за счёт разрастания опухолевой ткани и компрессионного сдавления окружающих органов;
- появление опухолевых инфильтратов в лёгких и ЦНС, которые проявляются неврологической симптоматикой (параличом, парезом и энцефалопатией) и пневмонией;
- при генерализации опухолевого процесса наступает почечная, печёночная и сердечно-лёгочная недостаточность;
- в связи с ослаблением иммунитета учащаются инфекционные заболевания, и появляются оппортунистические инфекции — их возбудителем являются организмы, не вызывающие патологий у здоровых людей.
Осложнения при неходжкинской лимфоме схожи, но есть некоторые особенности:
- чаще возникает лимфоматозный менингит;
- синдром верхней полой вены;
- двусторонняя непроходимость мочеточников;
- кишечная непроходимость из-за разрастания опухолевых масс в брыжейке кишки;
- ослабление мышечной активности конечностей, вплоть до полного обездвижения;
- компрессия спинного мозга;
- патологические переломы длинных костей.
Диагностика лимфомы
Как правило, при отсутствии системных проявлений заболевания и увеличении одного или нескольких лимфатических узлов проводят антибиотикотерапию. Если картина не меняется, необходимо выполнить ряд дополнительных обследований (рентген грудной клетки, КТ, УЗИ) и пункционную биопсию. Достоверный диагноз лимфомы можно поставить только на основании гистологии, полученной при биопсии лимфатического узла. Наиболее информативный способ — это забор изменённого лимфатического узла. Для определения подвида лимфомы и назначения химиотерапии необходимо провести полное морфологическое исследование с обязательным иммуногистохимическим анализом.
Перед взятием биопсии, помимо стандартного клинического обследования, необходимо исключить следующие факторы, влияющие на изменение лимфоузлов:
- хронический лимфолейкоз и острый лейкоз по общему анализу крови;
- учитывать, что лимфоцитоз может сопровождать инфекционную патологию, такую как ВИЧ, вирус Эпштейна-Бара, цитомегаловирус, вирусные гепатиты, токсоплазмоз и др.;
- опухоль вилочковой железы (выявляют методом компьютерной томографии);
- выяснить, не было ли в ближайшее время вакцинации и приёма лекарственных препаратов.
Диагноз ставится только по результатам гистологического исследования поражённого лимфатического узла. Анализ проводят методом аспирационной биопсии (взвесь клеток). Для этого под новокаином трепан-иглой (режущая игла, оснащённая пункционным пистолетом) берут столбик ткани поражённого органа, затем окрашивают и изучают под микроскопом.

Иногда этого бывает недостаточно, и морфологи просят предоставить для исследования часть или целый лимфатический узел. В таком случае под местной анестезией полностью удаляют конгломерат поражённых лимфоузлов [3][4].
Для постановки диагноза пользуются последней версией МКБ (Международная классификация болезней) с учётом стадийности, которая учитывает не только распространение опухоли по лимфатическим узлам и тканям за пределами лимфатической системы, но и общее состояние больного.
Также для диагностики лимфом применяют лучевые методы:
- рентгенография органов грудной клетки в двух проекциях используется при невозможности выполнения КТ, МРТ или позитронно-эмиссионной томографии;
- ультразвуковое исследование (УЗИ) периферических лимфатических, внутрибрюшных и забрюшинных узлов и органов брюшной полости — выполняют при невозможности выполнения КТ или МРТ (отсутствие оборудования в клинике или специалиста и боязни пациентом замкнутого пространства);
- компьютерная томография (КТ) грудной и брюшной полости — стандарт обследования пациентов с лимфомами;
- магнитно-резонансная томография (МРТ) шеи, грудной и брюшной полости зачастую позволяет чётко определить стадию заболевания;
- позитронно-эмиссионная томография (ПЭТ) и КТ всего тела с 18F-фтордезоксиглюкозой (ФДГ).
Визуализация лимфатических узлов и интерпретация полученных результатов во многом зависят от оборудования и специалиста, который проводит обследование. Для оценки динамики лечения лучше наблюдаться в одном медицинском центре и у того же специалиста. Это поможет уменьшить погрешность техники и влияние человеческого фактора.
Лечение лимфомы
При увеличенных лимфатических узлах категорически запрещено заниматься самолечением. Прогревать лимфоузлы нельзя, так как это может привести к распространению инфекции или генерализации опухолевого процесса. Также нельзя прикладывать лёд, так как это только усилит воспаление и ухудшит общее состояние пациента.
Лечение лимфомы Ходжкина заключается в использовании лучевой и лекарственной терапии, и их комбинации. При I и II стадиях болезни Ходжкина назначаются дакарбазин, винбластин, блеомицин и доксорубицин. Эти лекарства не вызывают серьёзных осложнений. Для полного излечения, которое возможно на этих стадиях у 95 % онкобольных, требуется не менее двух курсов этими препаратами; III и IV стадии лимфомы Ходжкина требуют 6-8 курсов лечения комплексом таких препаратов, как прокарбазин, винкристин, циклофосфамид, адриамицин, этопозид и бленоксан. Они также эффективны, но при их назначении имеется риск развития вторичного рака или лейкемии [7][10].
Лечение неходжкинской лимфомы. В лечении неходжкинских лимфом применяют лучевую терапию с/или химиотерапией. В ряде случаев проводят химиотерапию с последующей трансплантацией мезенхимальных стволовых клеток или костного мозга как источника стволовых клеток [8][9]. В последнее время обнадёживающие результаты лечения получены при использовании моноклональных антител. Следует отметить, что лечение в каждом случае врач подбирает индивидуально в зависимости от общего состояния пациента, сопутствующей патологии и варианта опухоли в соответствии со стандартами химиотерапии и лучевой терапии. В некоторых случаях (при большем локальном конгломерате узлов, значительно увеличенной селезёнке и др.) прибегают к хирургическому удалению поражённого органа [5][6]. В настоящее время разрабатываются молекулярно-генетические исследования опухолевых клеток, типирование, создание специфических сывороток и вакцин против каждого вида опухоли индивидуально для каждого пациента, но это медицина будущего и доступна пока единичным медицинским центрам.
Клинические рекомендации по определению эффективности лечения [4][5]
Эффективность лечения следует оценивать после 2-3 курсов химиотерапии при сохранении стабильной клинической картины не менее двух недель. С помощью УЗИ, КТ, МРТ или ПЭТ оценивают:
- динамику размеров лимфатических узлов;
- размеры опухоли при поражении печени или селезёнки;
Также проводят иммуногистохимическое исследование костного мозга для верификации опухолевых клеток. В зависимости от полученных данных, эффективность лечения расценивают как:
- полную ремиссию;
- частичную ремиссию;
- неуверенную полную ремиссию;
- частичную ремиссию и стабилизацию заболевания;
- рецидив.
Оценка эффективности также определяется в середине лечения с учётом размеров лимфатических узлов, количество поражённых лимфоузлов, размеров селезёнки, результата пункции костного мозга.
В литературе последних лет [11][12] появились исследования о прогностическом значении микроРНК (малые некодирующие молекулы РНК) и других маркеров, позволяющих на ранних стадиях и после курса лечения определить возможность рецидива. Эти современные маркеры являются наиболее чувствительными методами, но пока находятся на стадии клинических испытаний.
Прогноз. Профилактика
Прогноз при лимфоме Ходжкина зависит от формы и стадии заболевания:
- при локальных формах лимфомы Ходжкина с локализацией процесса над диафрагмой пятилетняя общая и безрецидивная выживаемость больных составляет при комплексной терапии около 90 %, десятилетняя и более — 80 %.
- при лимфоме Ходжкина III A стадии пятилетняя общая и безрецидивная выживаемость составляет более 80 %, при III Б стадии — около 60 %.
- при IV стадии после полихимиолучевого лечения пятилетняя общая выживаемость составляет около 45 %.
Хорошо выздоравливают молодые пациенты, особенно на ранних стадиях заболевания.
Неходжкинские лимфомы на ранних стадиях имеют относительно хороший прогноз. Современная терапия позволяет добиться более чем десятилетней выживаемости на ранних стадиях, но поздние стадии заболевания фактически не поддаются лечению и приводят к смерти.
В онкологической практике применяют таблицу прогнозирования выживаемости пациента с лимфомой [5][9].
| Международный прогностический индекс (МПИ): | ||
|---|---|---|
| Параметр | Благоприятный | Неблагоприятный |
| Возраст, годы | ≤60 | >60 |
| Общее состояние по шкале ECOG | 0-1 | 2-4 |
| Уровень ЛДГ в сыворотке | Нормальный | Повышен |
| Число экстранодальных очагов поражения | ≤1 | >1 |
| Стадия Ann Arbor | I-II | III-IV |
В правой колонке таблицы, представлены значения, характерные для неблагоприятного течения заболевания. Если каждый параметр принять за единицу, то рассчитывается МПИ следующим образом:
- 0-1 — низкая группа риска;
- 2 — промежуточная низкая;
- 3 — промежуточная высокая;
- 4 или 5 — высокая.
При достижении полной ремиссии регулярно проводится осмотр и опрос пациента, лабораторные исследования, рентгенологический контроль органов грудной клетки, УЗИ брюшной полости и периферических лимфатических коллекторов. Частота обследования:
- в течение первого года — каждые три месяца;
- на второй год — каждые шесть месяцев;
- в дальнейшем — ежегодно.
После проведённой химио- и лучевой терапией необходимо проверят
