Побочное действие общих анестетиков

С тех пор, как общий наркоз стал применяться в медицине, стало возможно проводить сложные операции без страха, что оперируемый скончается от болевого шока.
Однако последствия наркоза могут быть довольно опасными.
Разберемся, чем вреден общий наркоз для человека, как он влияет на организм, и какие осложнения может дать.
Почему пациенты опасаются анестезии

Многие пациенты не столько опасаются самого вмешательства, сколько беспокоятся, что их введут в состояние общего наркоза. Это обусловлено многочисленными мифами и слухами вокруг анестезии.
Действительно, в истории медицины описаны случаи, когда наркотическое вещество не оказывало нужного эффекта, а дополнительное введение препарата приводило к смерти пациента.
Второе, чем опасен общий наркоз, по мнению пациентов, это состояние, когда человек обездвижен, но всё осознаёт и чувствует боль. Такие страхи обоснованы, и на практике подобное происходит примерно в 0,2 % случаев.
Побочные действия анестетиков

Сегодня разработано множество различных анестетиков, и какие из них будут использованы в конкретном случае, определяет врач-анестезиолог. Его выбор зависит от вида и сложности хирургического вмешательства, наличия у пациента противопоказаний к тем или иным видам препаратов. Имеет значение опыт и квалификация анестезиолога.
Препараты для обезболивания хирургических вмешательств, обеспечивающие общую анестезию, являются сильнодействующими, имеют ряд побочных действий.
Около трети пациентов после общего наркоза чувствуют рвотные позывы, головокружение. Такие эффекты обусловлены понижением артериального давления. Пациенту необходимо отходить от анестезии лёжа, не принимая пищу.
Спутанность мыслей, необъективные оценки реальности, поведение, отклоняющееся от нормы, во время отхождения от наркоза более часто наблюдаются у пациентов преклонного возраста. По мере ослабления действия анестетика это состояние исчезает.
Тремор конечностей и головы, общая дрожь тела может быть спровоцирована некоторыми типами анестетиков. Это безопасно и продолжается не более получаса.
Последствия после наркоза могут проявиться зудящими ощущениями на коже. О таком эффекте нужно сообщить врачу, так как он в равной степени может свидетельствовать как об аллергии на медикаментозные препараты, так о побочном действии анестетиков морфинового ряда.
Болевые ощущения в спине после общей анестезии могут беспокоить пациента в период от нескольких часов до нескольких дней, и объясняются долгим пребыванием в положении лёжа. Мышечные боли чаще всего отмечают молодые мужчины. Некоторые пациенты жалуются на боли в горле. Они могут быть довольно продолжительными, причинять серьёзный дискомфорт.
Вредные побочные действия анестезирующих препаратов могут и не проявиться вовсе. Какие последствия будет иметь общий наркоз, нанесёт ли он вред или пройдёт бесследно, зависит от множества факторов. Анестезиологи стараются их учитывать, однако не всегда возможно предсказать, каково будет побочное действие анестезии.
Влияние анестетиков на организм

Вред общего наркоза не обсуждается, так как это общепризнанный факт, ведь для него используются сильнодействующие наркотические вещества. Разберемся, как действует общий наркоз, какие последствия для организма может иметь.
Наиболее опасные осложнения, которые могут возникать у людей от общей анестезии, это ухудшение функционирования центральной нервной системы, снижение когнитивных функций мозга. Кроме того, последствия общего наркоза могут привести к снижению работоспособности, расстройствам сна, ухудшению способности к запоминанию информации, нарушению концентрации внимания.
Вред наркоза иногда отмечается в течение продолжительного времени в виде панических атак, частичной потери памяти, нарушений функционирования сердца, печени и почек.
Такие осложнения анестезии обусловлены отмиранием нейронов мозга или микроинсультом вследствие снижения внутричерепного давления под действием анестетика. Усугубить астеническое последствие анестезии могут такие факторы, как преклонный возраст, наличие тяжёлых патологий, передозировка наркотического вещества.
Возможные последствия и осложнения общей анестезии

Разберемся, чем вреден наркоз более конкретно.
К наиболее опасным последствиям наркоза у взрослых и детей являются различной степени тяжести поражения центральной нервной системы, инфицирование лёгких, повреждение нервных волокон, глаз. При эндотрахеальном методе введения анестетика возможны механические повреждения ротовой полости и зубов.
Даже самый квалифицированный анестезиолог не может заранее предсказать, какое влияние окажет тот или иной препарат в конкретном случае. Для предупреждения осложнений и прогнозирования возможных последствий пациент проходит всестороннее обследование.
Однако развитие анафилактического шока исключить всё-таки нельзя. Примерно 5% случаев такой сильной аллергической реакции на анестетик приводит к летальному исходу.
Одним из самых неприятных осложнений считается возвращение сознания в процессе хирургического вмешательства. Состояние обездвиженности и болевые ощущения могут нанести вред психике, особенно если пациент ребенок.
Влияние на сердце

Сердечная недостаточность, недавно перенесённый инфаркт являются абсолютными противопоказаниями к проведению операции под общим наркозом. Оценивая риски, врачи сравнивают возможность сохранения жизни пациента при использовании радикальных методов лечения и без них.
Людям, у которых в анамнезе есть ишемическая болезнь, тахикардия, гипертония или гипотония, аритмия, кардиомиалгия или другие заболевания сердечно-сосудистой системы проходят тщательное обследование перед операцией.
Необходимо оценить, насколько хирургическое вмешательство опасно для человека с таким состоянием здоровья. Если принято решение о проведении операции для спасения жизни, анестезиолог должен определить наименее опасный препарат. Наркоз может влиять на ухудшение состояния сердечных больных.
Влияние на детей

Если операция требуется ребенку, её стараются отложить как можно дольше, чтобы он повзрослел, набрался сил. Однако есть случаи, когда медлить нельзя, и ребенок оказывается на операционном столе. Осложнения у детей старше двух лет наблюдаются довольно редко.
Когда есть возможность подождать, врачи не рекомендуют проводить операции в возрасте младше 4-5 лет. Сегодня уровень развития фармакологии таков, что препараты, применяемые в педиатрии, в том числе анестетики, имеют минимум побочных и вредных действий.
Наибольшую опасность общая анестезия представляет для людей преклонного возраста, в организме которых все процессы, в том числе регенерация, замедляются, и пациентов, страдающих тяжёлыми заболеваниями.
Если же человек в целом здоров, за исключением показаний к операции, не имеет лишнего веса, проблем с сердечно-сосудистой и центральной нервной системой, придерживается норм здорового образа жизни, то последствия будут минимальны.
Источник
Средства для наркоза, оказывая угнетающее влияние на центральную нервную систему, вызывают временную утрату сознания, угнетение всех видов чувствительности, снижение мышечного тонуса и рефлекторной активности при умеренном торможении жизненно важных центров продолговатого мозга. Препараты этой группы имеют важное значение для хирургии, развитие которой тесно связано с усовершенствованием обезболивания. Любая операция сопровождается сильными болевыми ощущениями, которые при недостаточном обезболивании могут вести к развитию болевого шока и гибели пациента. Средства для наркоза позволяют полностью снять болевые ощущения и их негативное влияние на организм, получить наиболее эффективное хирургическое обезболивание.
Впервые общий анестетик (азота закись) был применен Уэллсом в 1844 году при удалении зубов, но датой открытия наркоза считают 1886 год, когда Мортон публично продемонстрировал наркотическое действие эфира диэтилового. Известный хирург Н.И.Пирогов в том же году организовал массовое применение эфира перед операциями на поле боя.
По способу введения в организм все наркозные средства можно разделить на средства для ингаляционного наркоза, вводимые в организм через дыхательные пути, и для неингаляционного наркоза, вводимые, как правило, внутривенно.
Механизм действия наркозных препаратов заключается в блокаде межнейронной (синаптической) передачи возбуждения в центральной нервной системе. Единой теории, объясняющей их влияние на синаптическую передачу, нет. Данный эффект связывают с физико-химическими свойствами препаратов (способностью растворяться в липидах, содержание которых в нервной ткани повышено, нарушать окислительные процессы, адсорбироваться на мембране нервных клеток, образовывать нестойкие связи с белками нейронов центральной нервной системы, формировать с водой кристаллогидраты и т.д.). Несмотря на различие в биохимическом и физико-химическом механизме действия, все наркозные средства влияют на мембрану нейронов, изменяя ее проницаемость для ионов натрия и калия, нарушая процесс деполяризации. Это препятствует возникновению потенциала действия, в результате блокируется межнейронная передача возбуждения. Возможно, некоторые препараты действуют на пресинаптическом уровне, нарушая освобождение медиаторов, обусловливающих межнейронные контакты. В зависимости от химического строения и физико-химических свойств различные препараты имеют особенности влияния на нейроны, что отражается на их фармакодинамике. Чувствительность синапсов различных отделов центральной нервной системы к наркозным средствам неодинакова: наиболее чувствительны к действию химических агентов синапсы восходящей активирующей системы ретикулярной формации ствола мозга и коры головного мозга, наиболее устойчивы – жизненно важные центры продолговатого мозга. Это обусловливает наличие нескольких периодов в течение наркоза – выделяют 4 основные стадии, выраженность которых может варьировать в зависимости от особенности действия отдельных общих анестетиков.
Сразу после введения в организм наркозного препарата развивается стадия анальгезии или оглушения (первая стадия). Она характеризуется резким снижением болевой чувствительности, спутанностью сознания, но контакт с пациентом сохраняется. Хотя продолжительность стадии анальгезии невелика (5-10 мин), она может использоваться для проведения кратковременных операций. Стадию анальгезии можно удлинить, используя перед наркозом (премедикация) болеутоляющие и успокаивающие средства и поддерживая во вдыхаемом воздухе определенную концентрацию наркозного вещества.
В стадии возбуждения (вторая стадия) наблюдается полное выключение сознания, двигательное и речевое возбуждение, значительные колебания артериального давления, ритма сердца и дыхания. Возникновение этой стадии объясняется полным угнетением коры и снятием ее тормозящего влияния на нижележащие отделы, что сопровождается вторичным возбуждением подкорковых структур и повышением рефлекторной деятельности. В этот период нельзя проводить каких-либо хирургических вмешательств, так как возможна остановка дыхания, фибрилляция и остановка сердца.
В стадии хирургического наркоза (третья стадия) угнетение коры, подкорковых образований и спинного мозга приводит к полной утрате сознания, чувствительности, рефлексов, расслаблению скелетной мускулатуры, нормализуется артериальное давление, урежается пульс, дыхание становится ритмичным, поскольку сохраняется функция жизненно важных центров продолговатого мозга. Большинство хирургических вмешательств проводится в этой стадии.
Сразу после прекращения вдыхания наркозного средства начинается стадия пробуждения, при этом функции центральной нервной системы восстанавливаются в обратной последовательности. При передозировке наркозных препаратов наблюдается глубокое угнетение жизненно важных центров продолговатого мозга, нарушается дыхание и кровообращение, резко расширяются зрачки, смерть наступает от паралича дыхательного центра и остановки дыхания.
В чистом виде мононаркоз в настоящее время применяется редко. Для более быстрого введения в наркоз и уменьшения осложнений от применения общих анестетиков используется комбинированный и смешанный наркоз, а для подготовки к операции проводится премедикация – пациенту назначают успокаивающие и болеутоляющие препараты. При смешанном наркозе используют сочетание некоторых средств для наркоза (например, эфир, фторотан и закись азота), что позволяет снизить дозу каждого из них, а следовательно, и токсичность. Комбинированный наркоз основан на сочетании неингаляционного и ингаляционного наркоза. Современный уровень развития анестезиологии (науки, изучающей возможные варианты обезболивания) позволяет подбирать индивидуальную схему премедикации и наркоза для каждого пациента с учетом его общего состояния, характера заболевания и планируемого объема хирургического вмешательства. Наркотизирование проводит врач- анестезиолог, который должен в совершенстве владеть приемами реаниматологии, то есть восстановления утраченных жизненных функций, что может наблюдаться во время наркотизирования и проведения операций. Врач-анестезиолог должен не только снять боль, но и позволить хирургу провести операцию с наименьшими нарушениями функций различных органов и систем, с наименьшими затратами жизненных сил организма пациента. Активность общих анестетиков повышается введением успокаивающих и болеутоляющих препаратов. Для расслабления скелетной мускулатуры используют миорелаксанты, для устранения отрицательных вагусных рефлексов применяют М-холиноблокаторы (атропин и другие). При необходимости в предоперационную терапию включают сердечно-сосудистые, антигистаминные и другие препараты.
К средствам для наркоза предъявляют определенные требования. Они должны иметь высокую наркотическую активность, обеспечивать хорошую управляемость наркозом, то есть давать быстрое введение (желательно без стадии возбуждения) и выведение из наркоза. хорошую регулируемость его глубины, малую токсичность, большую широту наркотического действия, т.е. достаточный диапазон между концентрацией препарата в крови, вызывающей стадию наркоза, и концентрацией, вызывающей угнетение жизненно важных центров продолговатого мозга.
- 2.1.3.1.1. Средства для ингаляционного наркоза
- 2.1.3.1.2. Средства для неингаляционного наркоза
Источник

Анестетики разделяют на:
- Местные
- Общие:
а) ингаляционные – летучие жидкости и газы
б) неингаляционные (внутривенные)
Таблица 1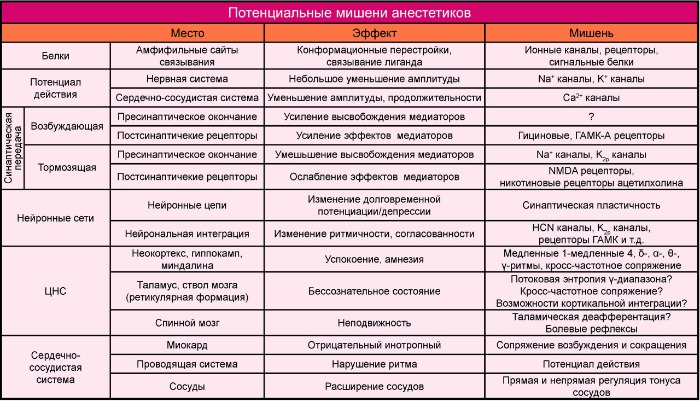
1. Местные анестетики
Местные анестетики обратимо снижают возбудимость чувствительных нервных окончаний и блокируют проведение афферентных импульсов в нервных стволах в зоне непосредственного применения, используются для устранения боли.
Первый препарат этой группы — кокаин, был выделен в 1860 г. Альбертом Ньюманом из листьев южноамериканского кустарника Erythroxylon coca. Ньюман, как многие химики прошлого, попробовал новое вещество на вкус и отметил онемение языка. Профессор Военно-медицинской академии Санкт-Петербурга Василий Константинович Анреп в 1879г. подтвердил способность кокаина вызывать анестезию. В экспериментах на лягушках он обнаружил, что кокаин влияет «парализующим образом» на окончания чувствительных нервов. В. К. Анреп исследовал действие кокаина на себе: инъекция кокаина в дозе 1 — 5 мг под кожу сопровождалась полной анестезией — укол булавкой, прижигание тлеющей спичкой не вызывали боли. Аналогичный эффект наблюдался при закапывании раствора кокаина в глаз и нанесении его на слизистую оболочку языка.
Местные анестетики классифицируют на сложные эфиры (анестезин, дикаин, новокаин) и замещенные амиды (лидокаин, тримекаин, бупивакаин). Местные анестетики — сложные эфиры подвергаются гидролизу псевдохолинэстеразой крови и действуют в течение 30 — 60 мин. Их эффект пролонгируют антихолинэстеразные средства (прозерин). Продукт гидролиза — n-амино-бензойная кислота ослабляет бактериостатическое влияние сульфаниламидов. Замещенные амиды кислот инактивируются монооксигеназной системой печени в течение 2 — 3 ч. Бупивакин вызывает местную анестезию продолжительностью 3 — 6 ч, после ее прекращения длительно сохраняется анальгетический эффект.
С точки зрения практического применения анестетики подразделяют на следующие группы:
- Средства, применяемые для поверхностной (терминальной) анестезии: Кокаин, Дикаин, Анестезин, Пиромекаин
- Средства, применяемые преимущественно для инфильтрационной и проводниковой анестезии: Новокаин, Бупивакаин
- Средства, применяемые для всех видов анестезии: Лидокаин, Тримекаин
Механизм действия
Местные анестетики представляют собой третичные азотистые основания. Они состоят из гидрофильной и липофильной частей, соединенных эфирной или амидной связями. Механизм действия определяет липофильная часть, имеющая ароматическую структуру. Для нанесения на слизистые оболочки и кожу и парентерального введения применяют водные растворы хлористоводородных солей местных анестетиков. В слабощелочной среде тканей (рН=7,4) соли гидролизуются с освобождением оснований. Основания местных анестетиков растворяются в липидах мембран нервных окончаний и стволов, проникают к внутренней поверхности мембраны, где превращаются в ионизированную катионную форму.
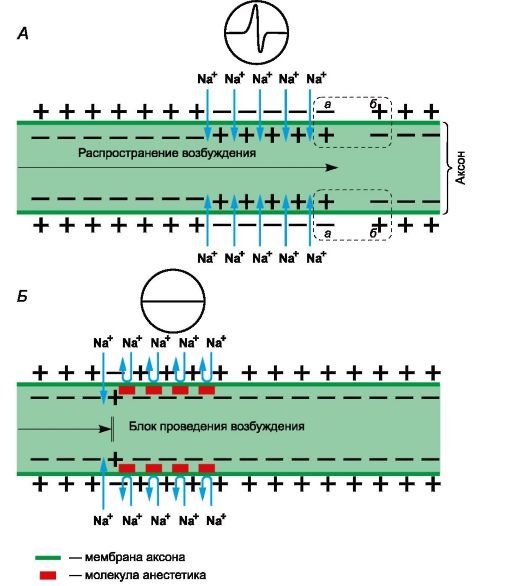 Рисунок 1 | Механизм действия местных анестетиков
Рисунок 1 | Механизм действия местных анестетиков
Рецепторы для местных анестетиков локализованы в S6-сегменте IV домена внутриклеточной части натриевых каналов. Связываясь с рецепторами, катионы местных анестетиков пролонгируют инактивированное состояние натриевых каналов, что задерживает развитие следующего потенциала действия. Местные анестетики не взаимодействуют с закрытыми каналами в период потенциала покоя. Таким образом, в зоне нанесения местных анестетиков не развиваются потенциалы действия, что сопровождается блоком проведения нервных импульсов. Избирательное влияние местных анестетиков на чувствительные афферентные нервы обусловлено генерацией в них длительных (более 5 мс) потенциалов действия с высокой частотой.
В первую очередь местные анестетики блокируют безмиелиновые С и миелиновые Аδ и Аβ волокна (афферентные пути, проводящие болевые и температурные раздражения; вегетативные нервы). На волокна, окруженные миелиновой оболочкой, местные анестетики действуют в области перехватов Ранвье. Толстые миелиновые волокна (афферентные пути, проводящие тактильные раздражения; двигательные нервы) слабее реагируют на местные анестетики. Кроме того, устойчивость двигательных нервов к анестезии обусловлена низкочастотными короткими (менее 5 мс) потенциалами действия. В очаге воспаления в условиях ацидоза нарушаются диссоциация хлористоводородных солей местных анестетиков и образование их свободных липидорастворимых оснований, поэтому обезболивающее влияние утрачивается. Например, местная анестезия может оказаться неэффективной при удалении зуба в случае тяжелого периодонтита.
2. Общие анестетики
2.1. Ингаляционные анестетики
2.1.1 Летучие жидкости
Теории механизма действия общих анестетиков
Эффекты ингаляционных анестетиков не могут быть объяснены одним молекулярным механизмом. Скорее всего многокомпонентное действие каждого анестетика реализуется через множество мишеней. Тем не менее, эти эффекты сходятся на ограниченном числе изменений, лежащих в основе физиологических эффектов. На данный момент существуют липидная и белковая теории анестезии, но ни одна из них пока не описывает последовательность событий, происходящих от взаимодействия молекулы анестетика и ее мишеней до физиологических эффектов.
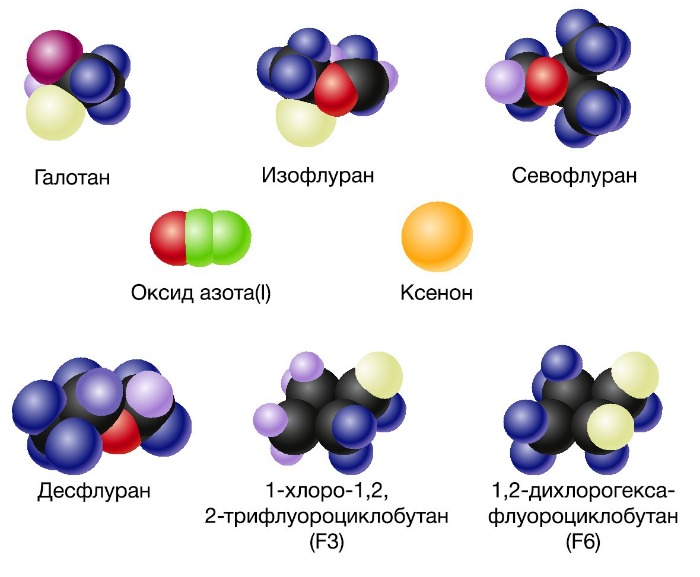 Рисунок 2 | Ингаляционные анестетики
Рисунок 2 | Ингаляционные анестетики
Активность ингаляционных анестетиков оценивают по минимальной альвеолярной концентрации (МАК). Доза, создающая 1 МАК, предотвращает у половины пациентов движения в ответ на хирургическое вмешательство. Сила общих анестетиков коррелирует с их растворимостью в жирах, что говорит о важности взаимодействия с гидрофильными мишенями. В частности, обнаружение связи между силой анестетика и его липофильностью (правило Мейер-Овертона) дало начало липидной теории механизма действия анестетиков. Липидная теория анестезии утверждает, что анестетики растворяются в двойном липидном слое биологических мембран и вызывают анестезию, достигая критической концентрации в мембране. Наиболее усложненные версии липидной теории требуют, чтобы молекулы анестетиков вызывали пертурбацию (изменение свойств) мембраны.
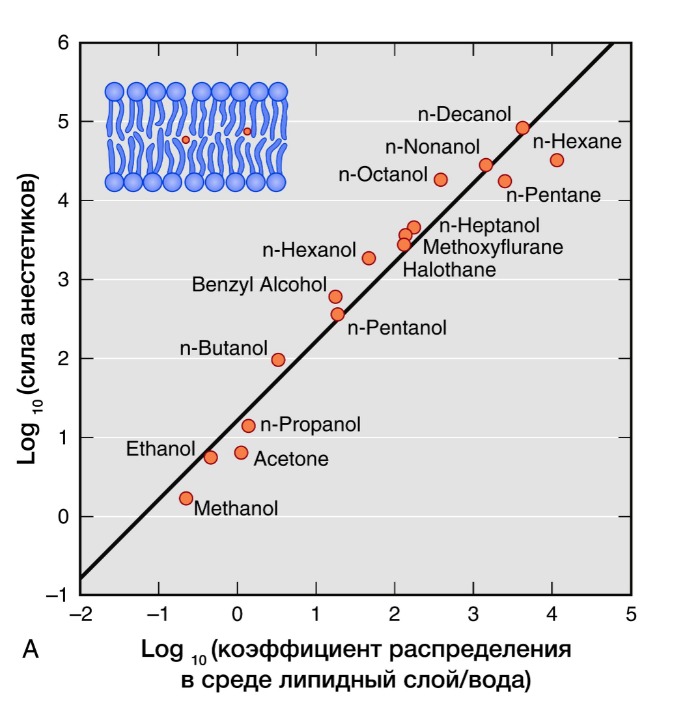 Рисунок 3 | Правило Мейер-Овертона
Рисунок 3 | Правило Мейер-Овертона
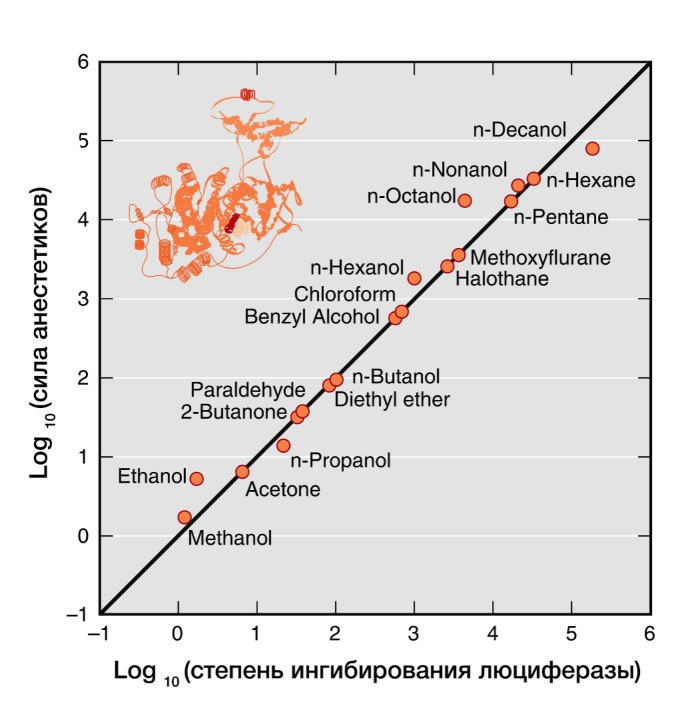 Рисунок 4 | В 20 веке было показано, что сила общих анестетиков коррелируют с их способностью ингибировать активность растворимого фермента люциферазы, который физиологически не является мишенью анестетиков, но служит в качестве безлипидной модели белковой молекулы для связывания анестетика.
Рисунок 4 | В 20 веке было показано, что сила общих анестетиков коррелируют с их способностью ингибировать активность растворимого фермента люциферазы, который физиологически не является мишенью анестетиков, но служит в качестве безлипидной модели белковой молекулы для связывания анестетика.
Современные факты позволяют утверждать, что белки в большей степени, чем липиды, являются молекулярными мишенями для действия анестетиков. Взаимодействие анестетиков с гидрофобными участками белков также объясняет правило Мейер-Овертона. Прямое взаимодействие молекул анестетиков с белками позволяет объяснить исключения из этого правила, так как любые участки связи с белком определяются как размером и формой молекулы, так и растворимостью. Многочисленные физические методы (рентгенодифракция, ЯМР-спектроскопия) подтверждают, что общие анестетики действуют путем непосредственного связывания с амфифильными полостями белковых молекул, а размер связанного участка объясняет эффект «обрубания» свойства (более длинные спирты теряют свойства анестетика).
Механизм действия
Таким образом, общие анестетики изменяют физико-химические свойства липидов мембран нейронов и нарушают взаимодействие липидов с белками ионных каналов. При этом уменьшается транспорт в нейроны ионов натрия, сохраняется выход менее гидратированных ионов калия, в 1,5 раза возрастает проницаемость хлорных каналов, управляемых ГАМК-А рецепторами. Итогом этих эффектов становится гиперполяризация с усилением процессов торможения. Общие анестетики подавляют вход в нейроны ионов кальция, блокируя Н-холинорецепторы и NMDA-рецепторы глутаминовой кислоты; снижают подвижность Са2+ в мембране, поэтому препятствуют кальций-зависимому выделению возбуждающих нейромедиаторов. Наиболее чувствительны к действию общих анестетиков полисинаптические системы ЦНС — кора больших полушарий (1013 – 1014 синапсов), таламус, ретикулярная формация, спинной мозг. К наркозу устойчивы дыхательный и сосудодвигательный центры продолговатого мозга.
Летучие ингаляционные анестетики:
- постсинаптически усиливают тормозящую передачу путем потенциирования лиганд-управляемых ионных каналов, активируемых ГАМК и глицином;
- экстрасинаптиески путем усиления ГАМК-рецепторов и ионных токов утечки;
- пресинаптически за счет повышения базального высвобождения ГАМК.
Ингаляционные анестетики подавляют возбуждающую синаптическую передачу путем снижения высвобождения глутамата и постсинаптически путем ингибирования ионотропных глутаматных рецепторов. Парализующий эффект местных анестетиков включает действие на спинной мозг, в то время как седация/наркоз и амнезия включают супраспинальные механизмы памяти, сна и сознания.
2.1.2. Газовый наркоз
В анестезиологии широко применяют ингаляционный газовый анестетик азота закись (N2O). В конце 1980-х гг. в зарубежную анестезиологическую практику вошел инертный газ ксенон.
Азота закись представляет собой бесцветный газ характерного запаха, хранится в металлических баллонах под давлением 50 атм в жидком состоянии, не горит, но поддерживает горение. Ее смеси с анестетиками группы летучих жидкостей в определенных концентрациях взрывоопасны. В субнаркотических концентрациях (20 — 30 %) азота закись вызывает эйфорию (веселящий газ) и сильную анальгезию. В концентрации 20 % обеспечивает обезболивание в такой же степени, как 15 мг морфина. Закись азота на ГАМК-А рецепторы не влияет. Используется только в комбинациях, так как МАК составляет 104 %.
Инертный газ ксенон считают лучшей альтернативой азота закиси, так как он обладает более выраженным наркозным действием, индифферентностью и экологической безопасностью. Способность ксенона вызвать наркоз была открыта в связи с практикой глубоководных погружений и развитием гипербарической физиологии. Ксенон бесцветен, не горит и не обладает запахом, при соприкосновении со слизистой оболочкой рта создает на языке ощущение горьковатого металлического вкуса. Отличается низкой вязкостью и высокой растворимостью в липидах, выводится легкими в неизмененном виде. Разработана технология ксенонсберегающей анестезии с включением минимального потока и системы рециклинга для повторного многократного использования газа. Такая технология успешно решает важную в практическом отношении проблему дефицита и дороговизны ксенона. В механизме наркозного эффекта ксенона имеют значение блокада циторецепторов возбуждающих нейромедиаторов — Н-холинорецепторов, NMDA-рецепторов глутаминовой кислоты, а также активация рецепторов тормозящего нейромедиатора глицина. При взаимодействии с циторецепторами ксенон выступает как протонсвязывающий кластер и образует комплексы с катионами НСО+, NH2+, HNCH+. Ксенон проявляет свойства антиоксиданта и иммуностимулятора, снижает выделение гидрокортизона и адреналина из надпочечников.
2.2. Неингаляционные (внутривенные) наркозные средства подразделяют на три группы:
Препараты короткого действия (3 — 5 мин)
- пропанидин (эпонтол, сомбревин)
- пропофол (диприван, рекофол)
Препараты средней продолжительности действия (20 — 30 мин)
- кетамин (калипсол, кеталар, кетанест)
- мидазолам (дормикум, флормидал)
- гексенал (гексобарбитал-натрий)
- тиопентал-натрий (пентотал)
Препараты длительного действия (0,5 — 2 ч)
- натрия оксибутират
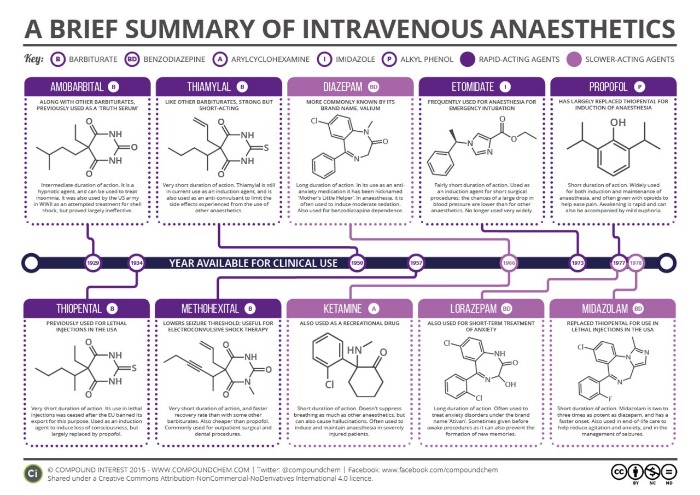 Рисунок 5 | Общие анестетики для внутривенного введения
Рисунок 5 | Общие анестетики для внутривенного введения
Механизм действия
Наиболее широко используемым внутривенный анестетиком является пропофол. Его механизм действия связан с увеличение хлорной проводимости ГАМК рецепторов.
Метогекситал по скорости наступления и выхода из наркоза близок к пропофолу.
Барбитураты использовались для анестезии до введения в практику пропофола. Тиопентал вызывает быстрое наступление и быстрый выход из наркоза при разовом введении, но он быстро накапливается при повторном или пролонгированном введении и таким образом замедляет выход из анестезии. Барбитураты являются лигандами барбитуратных рецепторов. В малых дозах они аллостерически усиливают действие ГАМК на ГАМК А-рецепторы . При этом удлиняется открытое состояние хлорных каналов, возрастает вход в нейроны анионов хлора, развиваются гиперполяризация и торможение. В больших дозах барбитураты прямо повышают хлорную проницаемость мембран нейронов. Кроме того, они тормозят высвобождение возбуждающих медиаторов ЦНС — ацетилхолина и глутаминовой кислоты, блокируют АМРА-рецепторы (квисквалатные рецепторы ) глутаминовой кислоты. Барбитураты обладают церебропротективными свойствами и могут быть использованы с такой целью.
Бензодиазепины используются в основном как анксиолитики и для седации с сохранением сознания.Все бензодиазепиновые рецепторы аллостерически усиливают кооперацию ГАМК с ГАМК А-рецепторами, что сопровождается повышением хлорной проводимости нейронов, развитием гиперполяризации и торможения. Реакция с бензодиазепиновыми рецепторами происходит только в присутствии ГАМК. Ремимазолам – самый молодой бензодиазепин, имеет очень короткое время действия из-за быстрой нейтрализации эстеразами плазмы.
Кетамин химически является производным фенциклидина. Синаптические механизмы действия кетамина многообразны. Он является неконкурентным антагонистом возбуждающих медиаторов головного мозга глутаминовой и аспарагиновой кислот в отношении NMDA-рецепторов. Эти рецепторы активируют натриевые, калиевые и кальциевые каналы мембран нейронов. При блокаде рецепторов нарушается деполяризация. Кроме того, кетамин стимулирует освобождение энкефалинов и β-эндорфина; тормозит нейрональный захват серотонина и норадреналина. Последний эффект проявляется тахикардией, ростом АД и внутричерепного давления. Кетамин расширяет бронхи. При выходе из кетаминового наркоза возможны бред, галлюцинации, двигательное возбуждение (эти нежелательные явления предупреждают введением дроперидола или транквилизаторов).Важным терапевтическим эффектом кетамина является нейропротективный. Как известно, в первые минуты гипоксии мозга происходит выброс возбуждающих медиаторов — глутаминовой и аспарагиновой кислот. Последующая активация NMDA-рецепторов, увеличивая во внутриклеточной среде концентрацию ионов натрия и кальция и осмотическое давление, вызывает набухание и гибель нейронов. Кетамин как антагонист NMDA-рецепторов устраняет перегрузку нейронов ионами и связанный с этим неврологический дефицит.
Самым новым внутривенным анестетиком является дексмедетомидин. Это высокоселективный агонист а2-адренорецепторов с седативными, симпатолитическими, снотворными и анальгетическими эффектами. Его основное действие – в качестве агониста на а2 рецепторы в голубом пятне.
Источники:
- Теории механизма действия – https://en.wikipedia.org/wiki/Theories_of_general_anaesthetic_action и https://www.esus.ru/php/content.php?id=744
- Венгеровский А.И., Лекции по фармакологии для врачей и провизоров 2007
- Харкевич, Фармакология изд. 10
- Miller’s anesthesia / [edited by] Ronald D. Miller ; associate editors, Neal H. Cohen, Lars I. Eriksson, Lee A. Fleisher, Jeanine P. Wiener-Kronish, William L. Young. — Eighth edition. 2015
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Источник
