Побочные эффекты миорелаксантов деполяризующего действия
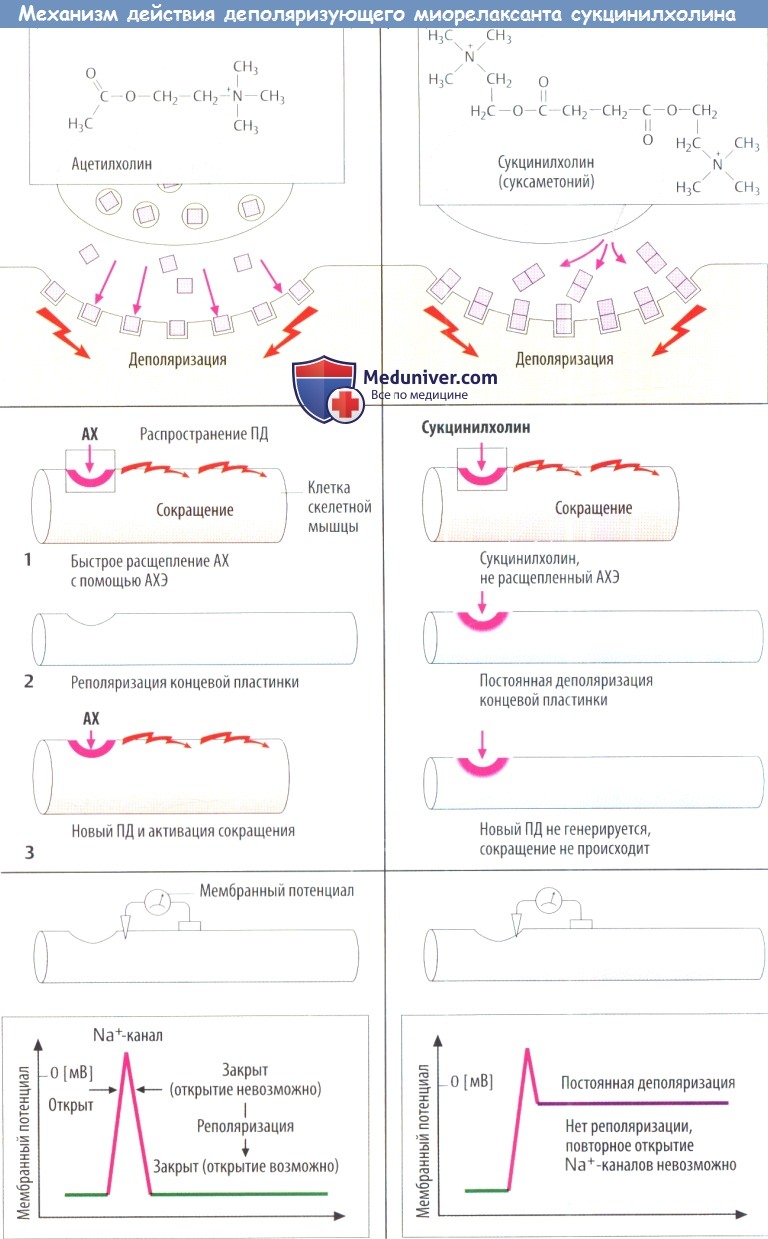
Механизм действия миорелаксантов и их эффекты
По мере развития медицины возникла необходимость искусственно вызывать вялый паралич скелетных мышц. Он необходим при искусственной вентиляции легких (ИВЛ). Длительную анестезию невозможно больше представить без расслабления мышц и вентиляции легких. Функцию концевой пластинки двигательного нерва можно обратимо нарушить на уровне рецепторов по двум механизмам.
Первый механизм заключается в том, что агонист после связывания с рецептором вызывает одиночный ПД в прилежащей мембране, но остается связанным, тем самым сохраняя деполяризацию концевой пластинки двигательного нерва. По такому механизму действуют деполяризующие миорелаксанты. Ко второй группе относятся недеполяризующие миорелаксанты, которые действуют как антагонисты АХ-рецепторов.
а) Деполяризующие миорелаксанты. Простейшее химическое вещество, которое парализует мышцы, вызывая длительную деполяризацию, — декаметоний:
(СН3)3N—(СН2)10—N+ (СН3)3.
По химическому строению представляет собой углеводородную цепь с двумя положительно заряженными атомами азота, расположенными на расстоянии 1 нм друг от друга. Метаболически стабильный декаметоний использовался в анестезии, но из-за неудовлетворительных фармакокинетических характеристик его применение прекращено. Он имеет типичную структуру для всех миорелаксантов. Такую же структуру имеет и суксаметоний (сукцинилдихолин).
Структура сукцинилхолина — две молекулы АХ. Он имеет сродство к N-холинорецептору, но не разрушается специфической АХЭ. Неспецифическая сывороточная холинэстераза расщепляет сукцинилхолин медленно,поэтому активная концентрация сохраняется в синаптической щели в течение 5-10 мин (для сравнения: продолжительность действия АХ 1-2 мс).
Новый потенциал действия (ПД) может быть вызван на концевой пластинке двигательного нерва только в том случае, если мембрана некоторое время находится в невозбужденном состоянии, допуская реполяризацию. Возникновение ПД связано с открытием белковых Na+-каналов, что позволяет ионам Na+ проходить через сарколемму и вызывать деполяризацию.
Через несколько миллисекунд Na+-каналы автоматически закрываются (происходит их инактивация) мембранный потенциал возвращается до значения, наблюдаемого в состоянии покоя, и генерация ПД прекращается. До тех пор пока не произошла полная реполяризация мембраны, открытие Na+-каналов и, следовательно, образование ПД невозможны.
Быстрое разрушение АХ, высвобождаемого АХЭ, способствует реполяризации концевой пластинки двигательного нерва и, следовательно возвращает возбудимость Na+-каналам в окружающей сарколемме. Под влиянием сукцинилхолина происходит стойкая деполяризация концевой пластинки двигательного нерва и прилегающих областей мембраны. Поскольку Na+-каналы остаются инактивированными, на прилежащей мембране ПД не образуется.
Побочные эффекты сукцинилхолина — повышение концентрации К+ в сыворотке, что может привести к нарушению функции сердца, подъему АД и тахикардии вследствие ганглионарной стимуляции. Сукцинилхолин стимулирует сокращение тонических волокон наружных мышц глаза и повышает внутриглазное давление.
Поэтому сукцинилхолин нельзя применять перед операциями на глазном яблоке. Кроме того, в хронически денервированных мышцах развиваются контрактуры, т. к. после повреждения двигательного нерва на неповрежденной поверхности денервированной скелетной мышцы появляются АХ-рецепторы. Подобная контрактура в сочетании с потерей К+ может наблюдаться у пациентов, которым выполняют корректирующую операцию через определенное время послетравмы.
К преимуществам сукцинилхолина относится его очень быстрое начало действия. В последнее время созданы быстродействующие недеполяризующие миорелаксанты, поэтому использование сукцинилхолина сократилось. Сукцинилхолин служит основным миорелаксантом для экстренной интубации.
Деполяризация концевой пластинки двигательного нерва вызывает образование распространяющегося ПД в мембранах окружающих мышечных клеток, что приводит к сокращению мышечного волокна. Непродолжительное время после в/в инъекции наблюдаются мелкие подергивания мышц.

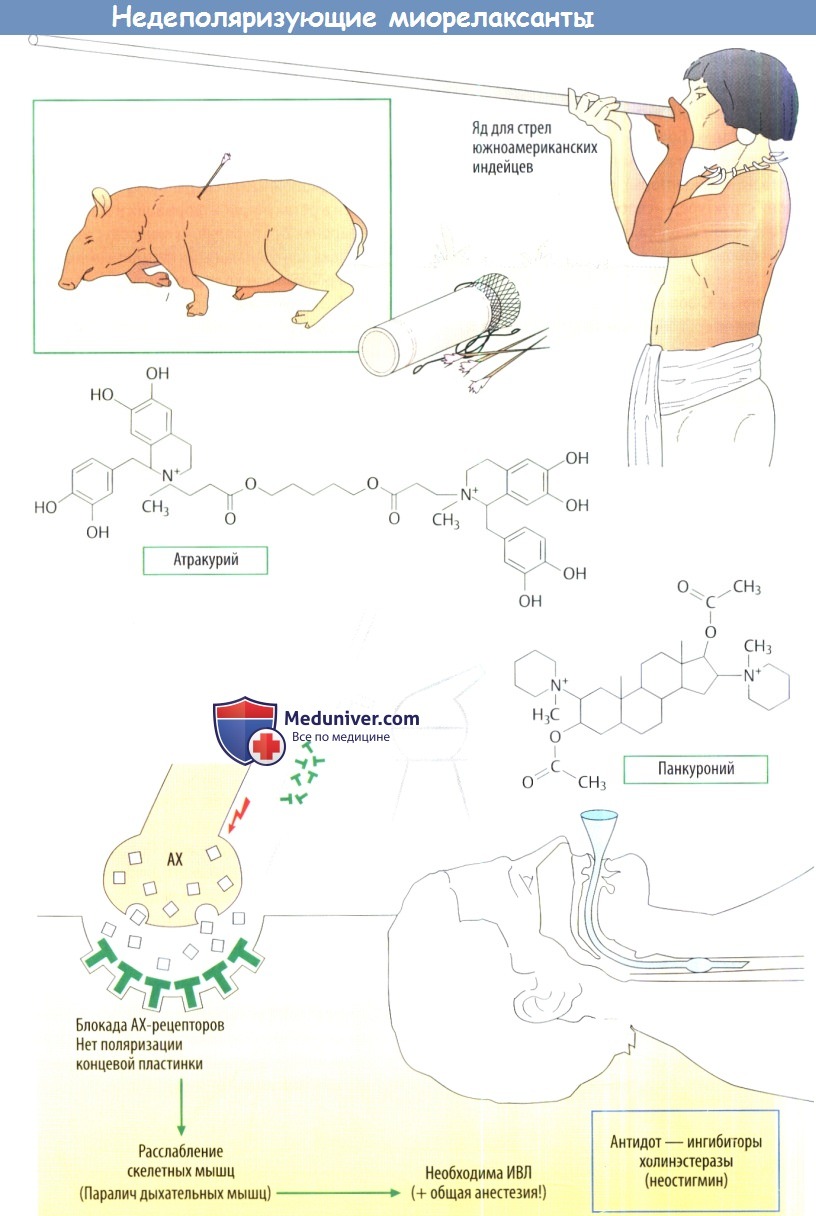
б) Недеполяризующие миорелаксанты. Яды, парализующие мускулатуру, давно известны и сыграли определенную роль в истории человечества. Коренные народы Южной Америки при охоте использовали отравленные стрелы, яд которых вызывал мышечный параличу животных. Тем не менее мясо убитых животных было неопасно для употребления, т. к. эти мышечные яды не всасываются в ЖКТ.
Подобные миорелаксанты имеют более сложную химическую структуру, чем декаметоний. В молекуле недеполяризующих миорелаксантов также имеется два ключевых положительно заряженных атома азота, но они расположены в системе колец. Эти два азотсодержащих кольца соединены либо длинной алифатической цепью, либо стероидной структурой. Формулы двух синтетических миорелаксантов показаны на рис. А. Эти крупные молекулы имеют высокое сродство к N-холинорецепторам, но не обладают собственной активностью, т. е. это чистые антагонисты.
Компонент яда кураре, D-тубокурарин, больше не используется в анестезии из-за неприемлемых побочных эффектов: высвобождение гистамина с падением АД, бронхоспазм и повышение секреции в бронхиальном древе. Также наблюдается ганглиоблокирующий эффект. Новыесинтетические миорелаксанты переносятся лучше. Они различаются по своим фармакокинетическим свойствам, например скорости начала и продолжительности действия.
В хирургии используются следующие препараты: панкуроний (длительного действия), векуроний (среднего действия), мивакурий (короткого действия), рокуроний (быстрое начало действия) и атракурий (расщепляется самопроизвольно после введения и не требует метаболической деградации, что важно для пациентов с заболеваниями печени).
Продолжительность действия недеполяризующих миорелаксантов можно сократить при использовании ингибиторов АХЭ, например неостигмина. АХ, секретируемый концевой пластинкой двигательного нерва, не расщепляется и накапливается в синаптической щели. Отношение антагониста к агонисту смещается в сторону нейромедиатора.
Наконец, следует отметить, что миорелаксанты не проникают в ЦНС. Это означает, что после введения миорелаксантов пациент будет находиться в сознании, однако возможна острая гипоксия вследствие паралича дыхательных мышц. В это время общение с пациентом невозможно из-за паралича всех мышц. При использовании миорелаксантов необходима анестезия и ИВЛ.
При обсуждении миорелаксантов необходимо упомянуть про яд, который вызывает паралич мышц путем блокады высвобождения АХ из концевой пластинки двигательного нерва. Это ботулинический токсин, выделяемый Clostridium botulinum. После прохождения через пресинаптическую мембрану он нарушает процесс слияния везикул, содержащих АХ, с мембраной. Ботулинический токсин — чрезвычайно сильный яд. Эффект длится долгое время, т. к. повреждение концевой пластинки двигательного нерва необратимо.
Восстановление иннервации происходит за счет роста новой концевой ветви аксона. Этот токсин используется в качестве лекарственного средства. Он вводится в мышцы при лечении болезненных мышечных спазмов, например блефароспазма. Токсин также используется в косметической медицине для модной в настоящее время подтяжки кожи лица.
в) Влияние на сократительную систему. ПД на короткое время деполяризует плазмолемму мышечных клеток, а также распространяется на саркоплазматический ретикулум. Это вызывает высвобождение Са2+ из саркоплазматического ретикулума, что приводит к укорочению актомиозина. Данный процесс известен как электромеханическое сопряжение. Он ингибируется дантроленом, который используют для лечения болезненных спазмов мышц и злокачественной гипертермии.
– Также рекомендуем “Лекарства для лечения боли и ее уменьшения”
Оглавление темы “Фармакология лекарств”:
- Лекарства при повышенной кислотности желудка и лечения язвы
- Слабительные препараты для лечения запора и нормализации стула
- Лекарства от поноса – для лечения диареи
- Лекарства влияющие на двигательную систему
- Механизм действия миорелаксантов и их эффекты
- Лекарства для лечения боли и ее уменьшения
- Механизм действия простагландинов и их эффекты
- Механизм действия жаропониющих обезболивающих и НПВС
- Механизм местной анестезии и эффекты местных анестетиков
- Механизм действия опиоидов – морфина и трамадола
Источник
Мышечные релаксанты или миорелаксанты — это препараты, приводящие к расслаблению поперечно-полосатых мышц.
Классификация миорелаксирующих веществ.
Общепринятой является классификация, в которой миорелаксанты разделяют на центральные и периферические. Механизм действия этих двух групп различается уровнем воздействия на синапсы. Центральные мышечные релаксанты влияют на синапсы спинного и продолговатого мозга. А периферические — непосредственно на синапсы, передающие возбуждение мышце. Кроме вышеперечисленных групп существует классификация, разделяющая миорелаксанты в зависимости от характера воздействия.
Центральные миорелаксанты не получили распространения в анестезиологической практике практике. А вот препараты периферического действия активно применяются для расслабления скелетной мускулатуры.
Выделяют:
- деполяризующие миорелаксанты;
- антидеполяризующие миорелаксанты.
Существует также классификация по длительности действия:
- ультракороткие — действуют 5-7 минут;
- короткие — менее 20 минут;
- средние — менее 40 минут;
- длительного действия — более 40 минут.
Ультракороткими являются деполяризующие миорелаксанты: листенон, сукцинилхолин, дитилин. Препараты короткого, среднего и длительного действия в основном недеполяризующие миорелаксанты. Короткодействующие: мивакуриум. Среднего действия: атракуриум, рокурониум, цисатракуриум. Длительного действия: тубокурорин, орфенадрин, пипекуроний, баклофен.
Механизм действия миорелаксантов.
Недеполяризующие миорелаксанты еще называют недеполяризующими или конкурентными. Это название полностью характеризует их механизм действия. Миорелаксанты недеполяризующего типа конкурируют с ацетилхолином в синаптическом пространстве. Они тропны к одним и тем же рецепторам. Но ацетилхолин под воздействием холинэстеразы в считанные милисекунды разрушается. Поэтому он неспособен конкурировать с мышечными релаксантами. В результате такого действия ацетилхолин не способен воздействовать на постсинаптическую мембрану и вызвать процесс деполяризации. Цепь проведения неврно-мышечного импульса прерывается. Мышца не возбуждается. Чтобы прекратить блокаду и восстановить проводимость нужно ввести антихолинэстеразные препараты, например, прозерин или неостигмин. Эти вещества разрушат холинэстеразу, ацетилхолин не будет распадаться и сможет конкурировать с миорелаксантами. Предпочтение будет отдаваться естественным лигандам.
Механизм действия деполяризующих мышечных релаксантов заключается в создании стойкого деполяризующего эффекта, длящегося около 6 часов. Деполяризованная постсинаптическая мембрана неспособна принимать и проводить нервные импульсы, цепь передачи сигнала мышце прерывается. В данной ситуации использование антихолинэстеразных препаратов в качестве антидота будет ошибочным, так как накапливающийся ацетилхолин будет вызывать дополнительную деполяризацию и усиливать нейромышечную блокаду. Деполяризующие релаксанты имеют в основном ультракороткое действие.
Иногда миорелаксанты сочетают в себе действия деполяризующих и конкурентных групп. Механизм этого явления неизвестен. Предполагают, антидеполяризующие миорелаксанты имеют последействие, при котором мышечная мембрана приобретает стойкую деполяризацию и становится нечувствительной на некоторое время. Как правило — это препараты более длительного действия
Применение миорелаксантов.
Первыми миорелаксантами были алкалоиды некоторых растений, или кураре. Затем появились их синтетические аналоги. Не совсем правильно называть все мышечные релаксанты курареподобными веществами, так как механизм действия некоторых синтетических препаратов отличается от такового у алкалоидов.
Основной областью применения мышечных релаксантов стала анестезиология. В настоящее время клиническая практика не может обойтись без них. Изобретение этих веществ позволило вделать огромный скачок в области анестезиологии. Миорелаксанты позволили снизить глубину наркоза, лучше контролировать работу систем организма, создали условия для внедрения эндотрахеального наркоза. Для большинства операций основным условием является хорошее расслабление поперечно-полосатых мышц.
Влияние миорелаксантов на работу систем организма зависит от селективности воздействия на рецепторы. чем селективней препарат, тем меньше побочных действий со стороны органов он вызывает.
В анестезиологии применяются следующие мышечные релаксанты: сукцинилхолин, дитилин, листенон, мивакуриум, цисатракуриум, рокуроний, атракурий, тубокурарин, мивакуриум, пипекуроний и другие.
Кроме анестезиологии миорелаксанты нашли применение в травматологии и ортопедии для расслабления мышц при вправлении вывиха, перелома, а также при лечении заболеваний спины, связочного аппарата.
Побочные действия релаксантов.
Со стороны сердечно-сосудистой системы миорелаксанты могут вызывать учащение пульса и подъем давления. Сукцинилхолин имеет двоякое действие. Если доза малая, он вызывает брадикардию и гипотонию, если большая — противоположные эффекты.
Релаксанты деполяризующего типа могут приводить к гиперкалиемии, если уровень калия у пациента изначально был повышен. Это явление встречается у пациентов с ожогами, большими травмами, кишечной непроходимостью, столбняком.
В послеоперационном периоде нежелательными эффектами являются длительная мышечная слабость и боли. Это объясняется сохраняющейся деполяризацией. Длительное восстановление дыхательной функции может быть связано, как с действием мышечных релаксантов, так и с гипервентиляцией, обструкцией дыхательных путей или передозировкой декураризирующих препаратов (неостигмина).
Сукцинилхолин способен повышать давление в желудочках мозга, внутри глаза, в черепной коробке. Поэтому его применение в соответствующих операциях ограничено.
Миорелаксанты деполяризующего типа в сочетании с препаратами для общего наркоза могут вызывать злокачественное повышение температуры тела. Это жизнеугрожающее состояние, которое сложно купировать.
Основные названия препаратов и их дозы.
Тубокурарин. Доза тубокурарина, используемая для наркоза 0,5-0,6 мг/кг. Вводить препарат нужно медленно, в течение 3-х минут. Во время операции дробно вводят поддерживающие дозы по 0,05 мг/кг. Это вещество является натуральным алкалоидом кураре. Имеет тенденцию к снижению давления, в больших дозах вызывает значительную гипотензию. Антидотом Тубокурарина является Прозерин.
Дитилин. Этот препарат относится к релаксантам деполяризующего типа. Имеет короткое, но сильное действие. Создает хорошо контралируемое расслабление мышц. Основные побочные эффекты: длительно апное, подъем АД. Специфического антидота не имеет. Аналогичное действие имеют препараты листенон, сукцинилхолин, миорелаксан.
Диплацин. Неполяризующий миорелаксант. Действует около 30 минут. Доза, достаточная для одной операции — 450—700 мг. Никакие существенные побочные эффекты при его применении не наблюдались.
Пипекуроний. Доза для наркоза составляет 0,02 мг/кг. Действует длительно, в течение 1.5 часов. В отличие от остальных препаратов является более селективным и не действует на сердечно-сосудистую систему.
Эсмерон (рокуроний). Доза для интубации 0,45-0,6 мг/кг. Действует до 70 минут. Болюсные дозы во время операции 0,15 мг/кг.
Панкуроний. Известен под названием Павулон. Доза, достаточная, для введения в наркоз 0,08-0,1 мг/кг. Поддерживающая доза 0,01-0,02 мг/кг вводится каждые 40 минут. Имеет множественные побочные эффекты сос тороны сердечно-сосудистой системы, так как является неселективным препаратом. Может вызывать аритмию, гипертонию, тахикардию. Значительно влияет на внутриглазное давление. Может использоваться для операций Кесарева сечения, так как плохо проникает через плаценту.
Все эти препараты используются исключительно анестезиологами-реаниматологами при наличии специализированной дыхательной аппаратуры!
Источник
Миорелаксанты – препараты, предназначенные для расслабления поперечно-полосатой мускулатуры. Важным свойством мышечных релаксантов является их способность предотвращать рефлекторную активность всей произвольной мускулатуры. Это свойство имеет большое значение в хирургии и анестезиологии, так как мышечный тонус нередко мешает создавать оптимальные условия для хирургического вмешательства и проведения интубации.
Классификация мышечных релаксантов
Все мышечные релаксанты можно подразделить на деполяризующие и недеполяризующие. Кроме того, с клинической точки зрения целесообразно подразделять миорелаксанты на препараты ультракороткого действия (действуют 5-7 мин), короткого действия (продолжительность действия менее 20 мин), средней продолжительности (менее 40 мин) и миорелаксанты длительного действия (более 40 мин).
К деполяризующим мышечным релаксантам относятся препараты суксаметония – листенон, дитилин, сукцинилхолин. Они же являются миорелаксантами ультракороткого действия и отличаются друг от друга лишь входящей в состав солью.
К недеполяризующим миорелаксантам короткого действия относят мивакуриум. Недеполяризующими миорелаксантами средней продолжительности являются атракуриум, векурониум, рокурониум, цисатракуриум. Представителями недеполяризующих миорелаксантов длительного действия являются пипекуроний, панкурониум, тубокурарин.
Механизм действия деполяризующих миорелаксантов
Структура деполяризующих миорелаксантов сходна с молекулой ацетилхолина. При взаимодействии с Н-холинорецепторами препараты суксаметония вызывают потенциал действия мышечной клетки. Таким образом, подобно ацетилхолину деполяризующие миорелаксанты вызывают деполяризацию и стимуляцию мышечного волокна. Однако ацетилхолинэстераза на препараты суксаметония не действует, вследствие чего их концентрация в синаптической щели возрастает. Это приводит к длительной деполяризации концевой пластины и к миорелаксации.
Разрушение деполяризующих миорелаксантов происходит холинэстеразой плазмы.
Препараты суксаметония
При введении препаратов суксаметония полная нервно-мышечная блокада возникает в течение 30-40 секунд, что позволяет применять их для проведения интубации трахеи. Длительность нейро-мышечного блока – от 4 до 6 минут. Это время может увеличиться при количественной или качественной недостаточности плазменной холинэстеразы. Частота встречаемости недостаточности – 1:3000.
Иногда деполяризующие релаксанты могут вызвать вторую фазу блока – недеполяризующий блок. Тогда действие препаратов суксаметония приобретает непрогнозируемый эффект и длительность.
Побочные эффекты препаратов суксаметония
При использовании препаратов суксаметония следует иметь ввиду их высокий гистаминный эффект.
Побочное действие деполяризующих миорелаксантов на сердечно-сосудистую систему выражается в нарушениях ритма, колебаниях артериального давления и ЧСС. Причём препараты суксаметония чаще вызывают брадикардию.
Другим побочным эффектом, присущим всем деполяризующим миорелаксантам, являются фасцикуляции, по присутствии которых судят о начале действия препарата. Если появление фасцикуляций нежелательно, то перед введением суксаметония нужно провести прекурарезацию. Так называется метод введения недеполяризующего миорелаксанта ( к примеру, 1 мг аркурона) за 5 минут до введения суксаметония для профилактики побочных действия последнего.
Грозным побочным эффектом при применении препаратов суксаметония является гиперкалиемия. Если исходный уровень калия в норме, то этот побочный эффект не имеет клинического значения. При состояниях, сопровождающихся повышением уровня калия в крови (ожогах, обширных травмах, миопатии, столбняке, острой кишечной непроходимости) применение деполяризующих миорелаксантов может представлять угрозу для жизни.
Нередким побочным эффектом препаратов суксаметония являются мышечные боли в послеоперационном периоде.
Повышение давления в полости желудка, вызываемое мышечными релаксантами из группы деполяризующих препаратов, не увеличивает риск возникновения желудочного рефлюкса и лёгочной аспирации.
Сукцинилхолин повышает внутриглазное давление, что может ограничить его применение в офтальмологических операциях в отсутствии проведённой прекураризации.
Ультракороткие миорелаксанты увеличивают мозговой кровоток и внутричерепное давление, что также можно предотвратить прекураризацией.
Деполяризующие миорелаксанты могут вызывать злокачественную гипертермию.
Опасно введение суксаметония при миотонии – это может спровоцировать генерализованные сокращения (миоклонус).
Типичным представителем мышечных релаксантов, наиболее широко используемых в странах СНГ, является дитилин.
Дитилин выпускается в ампулах по 2 мл в виде 2% раствора. При внутривенном введении эффект развивается через 60 секунд и продолжается 5-10 минут, при внутримышечном – расслабление мускулатуры развивается через 2-4 минуты и длится 5-10 минут.
Дитилин с успехом применяется для интубации трахеи, при проведении бронхо- и эзофагоскопии, для кратковременных операций.
У взрослых рекомендуемая доза дитилина 2 мг/кг, у детей – до 2,5 мг/кг. Поддерживающая доза релаксанта – 1 мг/кг.
Механизм действия недополяризующих миорелаксантов
Молекулы недеполяризующих миорелаксантов конкурируют с молекулой ацецилхолина за право связаться с рецептором. При связывания миорелаксанта с рецептором последний теряет чувствительность к ацетилхолину, постсинаптическая мембрана находится в состоянии поляризации и деполяризации не происходит. Таким образом, недеполяризующие мышечные релаксанты по отношению к холиновым рецепторам можно назвать конкурентными антагонистами.
Недеполяризующие миорелаксанты не разрушаются ни ацетилхолинэстеразой, ни холинэстеразой крови.
Мивакуриум – мышечный релаксант, действующий до 20 минут. Его применение ограничено ввиду относительно частого побочного эффекта – высвобождения гистамина. Кроме того, зависимость его метаболизма от псевдохолинэстеразы не позволяет провести полную декураризацию антихолинэстеразными препаратами.
Появившись на рынке, мивакуриум не оправдал ожиданий производителей, хотя к его применению при определённых условиях всё же приходиться прибегать.
Атракуриум (тракриум) – мышечный релаксант средней продолжительности действия. Выпускается в ампулах по 2,5 и 5 мл. В 1 мл – 10 мг активного вещества.
Тракриум применяется как компонент общей анестезии при интубации трахеи. Особенно полезно его действие при хирургических вмешательствах и для облегчения проведения ИВЛ.
У взрослых тракриум применяют из расчёта 0,3-0,6 мг/кг. При необходимости дополнительного введения миорелаксанта доза должна быть рассчитана в количестве 0,1-0,2 мг/кг.
Детям в возрасте от двух лет атракурий назначается в тех же дозировках, что и взрослым. У детей младше двух лет миорелаксант применяют в расчёте 0,3-0,4 мг/ кг на фоне галотанового наркоза.
Восстановление проводимости после нервно-мышечной блокады, вызванной атракурием, происходит примерно через 35 минут.
Побочными эффектами применения тракриума могут быть:
- преходящее снижение артериального давления;
- гиперемия кожи;
- бронхоспазм;
- очень редко – анафилактические реакции.
Верокурониум – недеполяризующий миорелаксант стероидной структуры. Верокурониум мало влияет на высвобождение гистамина и отличается кардиостабильностью.
Цисатракуриум (нимбекс), являющийся стереоизомером атракурия, превосходит его по силе в три раза, хотя время наступления эффекта и его длительность примерно такая же, как и у атракурия.
Цисатракурий выпускается в виде ампул по 2,5 и 5 мл по 2 и 5 мг.
Как и для всех миорелаксантов, показаниями к применению цисатракурия служат интубация трахеи, поддержание расслабления мускулатуры, проведение ИВЛ.
Применяется нимбекс для интубации трахеи в дозе 0,15 мг/кг, поддерживающая доза- 0,1 мг/кг.
Рокурониум (эсмерон) – недеполяризующий миорелаксант средней продолжительности действия, положительной чертой которого является быстрота наступления эффекта. Кроме того, минимальное высвобождение гистамина и незначительный кардиоваскулярный эффект сделали рокуроний очень популярным препаратом в анестезиологии.
Эсмерон выпускается во флаконах по 5 мл, 10 мл и 25 мл. В 1 мл содержится 10 мг рокурония бромида.
Доза рокурония для интубации трахеи – 0,3-0,6 мг/кг, поддерживающая доза- 0,15 мг/кг.
Пипекуроний (ардуан, аркурон) относится к недеполяризующим миорелаксантам длительного действия.
Ардуан выпускается в ампулах по 2 мл (1 мл содержит 4 мг пипекурония бромида).
У взрослых пипекуроний применяется из расчёта 0,07-0,08 мг/кг, у детей – 0,08-0,09 мг/кг. Эффект препарата длится в течение 50-70 минут.
Из побочных явлений пипекурония следует отметить брадикардию, гипотонию, редко – анафилактические реакции.
Панкуриной (павулон) – выпускается в ампулах для внутривенного введения по 2 мл (1 мл содержит 2 мг панкурония бромида).
У взрослых и детей от четырёх недель панкуроний применяется в дозе 0,08-0,1 мг/кг. Препарат вызывает хорошую миорелаксацию для проведения интубации трахеи через 90-120 секунд.
Побочные действия со стороны сердечно-сосудистой системы, вызываемые панкуронием – незначительное повышение ЧСС и АД.
Тубокурарин выпускается в виде 1% раствора в ампулах по 1,5 мл.
В настоящее время тубокурарин практически не применяется из-за вызываемой им артериальной гипотонии и тахикардии, что является следствием повышенного высвобождения гистамина.
Начало действия тубокурарина через 60-90 секунд. Для интубации используют дозировку 0,5-0,6 мг/кг.
19.10.2010
Источник
