Порок сердца дмжп противопоказания

Дефект межжелудочковой перегородки – врожденная внутрисердечная аномалия, характеризующаяся наличием сообщения между правым и левым желудочками. Дефект межжелудочковой перегородки проявляется одышкой, отставанием в физическом развитии, быстрой утомляемостью, учащенным сердцебиением, наличием «сердечного горба». Инструментальная диагностика дефекта межжелудочковой перегородки включает проведение ЭКГ, ЭхоКГ, рентгенографии органов грудной клетки, вентрикулографии, аортографии, катетеризации камер сердца, МРТ. При дефектах межжелудочковой перегородки проводят радикальные (закрытие дефекта) и паллиативные (сужение легочной артерии) вмешательства.
Общие сведения
Дефект межжелудочковой перегородки (ДМЖП) – отверстие в перегородке, разделяющей полости левого и правого желудочка, наличие которого приводит к патологическому шунтированию крови. В кардиологии дефект межжелудочковой перегородки – наиболее часто встречающийся врожденный порок сердца (9–25% от всех ВПС). Частота критических состояний при дефекте межжелудочковой перегородки составляет около 21%. С одинаковой частотой порок обнаруживается у новорожденных мальчиков и девочек.
Дефект межжелудочковой перегородки может быть единственной внутрисердечной аномалией (изолированный ДМЖП) или входить в структуру сложных пороков (тетрады Фалло, общего артериального ствола, транспозиции магистральных сосудов, атрезии трехстворчатого клапана и др.). В ряде случаев межжелудочковая перегородка может отсутствовать полностью – такое состояние характеризуется как единственный желудочек сердца.
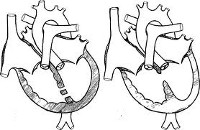
Дефект межжелудочковой перегородки
Причины дефекта межжелудочковой перегородки
Чаще всего дефект межжелудочковой перегородки является следствием нарушения эмбрионального развития и формируется у плода при нарушениях закладки органов. Поэтому дефекту межжелудочковой перегородки часто сопутствуют другие сердечные пороки: открытый артериальный проток (20%), дефект межпредсердной перегородки (20%), коарктация аорты (12%), стеноз устья аорты (5%), аортальная недостаточность (2,5—4,5%), недостаточность митрального клапана (2%), реже – аномальный дренаж легочных вен, стеноз легочной артерии и др.
В 25-50% случаев дефект межжелудочковой перегородки сочетается с пороками развития внесердечной локализации – болезнью Дауна, аномалиями развития почек, расщелиной твердого неба и заячьей губой.
Непосредственными факторами, вызывающими нарушение эмбриогенеза, выступают вредные воздействия на плод в I триместре гестации: заболевания беременной (вирусные инфекции, эндокринные нарушения), алкогольная и лекарственная интоксикации, ионизирующая радиация, патологическое течение беременности (выраженные токсикозы, угроза самопроизвольного прерывания беременности и пр.). Имеются данные о наследственной этиологии дефекта межжелудочковой перегородки. Приобретенные дефекты межжелудочковой перегородки могут являться осложнением инфаркта миокарда.
Особенности гемодинамики при дефекте межжелудочковой перегородки
Межжелудочковая перегородка образует внутренние стенки обоих желудочков и составляет примерно 1/3 площади каждого из них. Межжелудочковая перегородка представлена мембранозным и мышечным компонентами. В свою очередь, мышечный отдел состоит из 3-х частей – приточной, трабекулярной и отточной (инфундибулярной).
Межжелудочковая перегородка, наряду с другими стенками желудочков, принимает участие в сокращении и расслаблении сердца. У плода она полностью формируется к 4-5-ой неделе эмбрионального развития. Если этого по каким-либо причинам не происходит, в межжелудочковой перегородке остается дефект. Нарушения гемодинамики при дефекте межжелудочковой перегородки обусловлены сообщением левого желудочка с высоким давлением и правого желудочка с низким давлением (в норме в период систолы давление в левом желудочке в 4 – 5 раз выше, чем в правом).
После рождения и установления кровотока в большом и малом кругах кровообращения из-за дефекта межжелудочковой перегородки возникает лево-правый сброс крови, объем которого зависит от размеров отверстия. При небольшом объеме шунтируемой крови давление в правом желудочке и легочных артериях остается нормальным либо незначительно повышается. Однако при большом поступлении крови через дефект в малый круг кровообращения и ее возврате в левые отделы сердца, развивается объемная и систолическая перегрузка желудочков.
Значительное повышение давления в малом круге кровообращения при больших дефектах межжелудочковой перегородки способствует возникновению легочной гипертензии. Повышение легочно-сосудистого сопротивления взывает развитие сброса крови из правого желудочка в левый (обратного или перекрестного шунтирования), что приводит к артериальной гипоксемии (синдром Эйзенменгера).
Многолетняя практика кардиохиругов показывает, что наилучших результатов закрытия дефекта межжелудочковой перегородки можно добиться при сбросе крови слева направо. Поэтому при планировании операции тщательно учитываются гемодинамические параметры (давление, сопротивление и объем сброса).
Классификация дефекта межжелудочковой перегородки
Размер дефекта межжелудочковой перегородки оценивается, исходя из его абсолютной величины и сопоставления с диаметром аортального отверстия: маленький дефект составляет 1-3 мм (болезнь Толочинова–Роже), средний – равен примерно 1/2 диаметра аортального отверстия, большой – равен или превышает его диаметр.
С учетом анатомического расположения дефекта выделяют:
- перимембранозные дефекты межжелудочковой перегородки – 75% (приточные, трабекулярные, инфундибулярные) расположены в верхней части перегородки под аортальным клапаном, могут закрываться самопроизвольно;
- мышечные дефекты межжелудочковой перегородки – 10% (приточные, трабекулярные) – расположены в мышечном отделе перегородки, на значительном удалении от клапанной и проводящей систем;
- надгребневые дефекты межжелудочковой перегородки – 5% – расположены выше наджелудочкового гребня (мышечного пучка, отделяющего полость правого желудочка от его выносящего тракта), самопроизвольно не закрываются.
Симптомы дефекта межжелудочковой перегородки
Клинические проявления больших и малых изолированных дефектов межжелудочковой перегородки различны. Малые дефекты межжелудочковой перегородки (болезнь Толочинова—Роже) имеют диаметр менее 1 см и встречаются в 25-40% от числа всех ДМЖП. Проявляются нерезко выраженной утомляемостью и одышкой при нагрузке. Физическое развитие детей, как правило, не нарушено. Иногда у них определяется слабо выраженное куполообразное выпячивание грудной клетки в области сердца – «сердечный горб». Характерным клиническим признаком малых дефектов межжелудочковой перегородки служит аускультативно выявляемое наличие грубого систолического шума над областью сердца, который фиксируется уже на первой неделе жизни.
Большие дефекты межжелудочковой перегородки, имеющие размеры более 1/2 диаметра устья аорты или более 1 см, проявляются симптоматически уже в первые 3 месяца жизни новорожденных, приводя в 25-30% случаев к развитию критического состояния. При больших дефектах межжелудочковой перегородки отмечается гипотрофия, одышка при физической нагрузке или в покое, повышенная утомляемость. Характерны затруднения при кормлении: прерывистое сосание, частые отрывы от груди, одышка и бледность, потливость, пероральный цианоз. В анамнезе у большинства детей с дефектом межжелудочковой перегородки – частые респираторные инфекции, затяжные и рецидивирующие бронхиты и пневмонии.
В возрасте 3-4-лет, по мере нарастания сердечной недостаточности, у таких детей появляются жалобы на сердцебиение и боли в области сердца, склонность к носовым кровотечениям и обморокам. Транзиторный цианоз сменяется постоянным пероральным и акроцианозом; беспокоит постоянная одышка в покое, ортопноэ, кашель (синдром Эйзенменгера). На наличие хронической гипоксии указывают деформация фаланг пальцев и ногтей («барабанные палочки», «часовые стекла»).
При обследовании выявляется «сердечный горб», развитый в меньшей или большей степени; тахикардия, расширение границ сердечной тупости, грубый интенсивный пансистолический шум; гепатомегалия и спленомегалия. В нижних отделах легких выслушиваются застойные хрипы.
Диагностика дефекта межжелудочковой перегородки
К методам инструментальной диагностики дефекта межжелудочковой перегородки относятся ЭКГ, ФКГ, рентгенография грудной клетки, ЭхоКС, катетеризация камер сердца, ангиокардиография, вентрикулография.
Электрокардиограмма при дефекте межжелудочковой перегородки отражает перегрузку желудочков, наличие и степень выраженности легочной гипертензии. У взрослых больных могут регистрироваться аритмии (экстрасистолия, мерцание предсердий), нарушения проводимости (блокада правой ножки пучка Гиса, синдром WPW). Фонокардиография фиксирует высокочастотный систолический шум с максимумом в III-IV межреберье слева от грудины.
Эхокардиография позволяет выявить дефект межжелудочковой перегородки или заподозрить его по характерным нарушениям гемодинамики. Рентгенография органов грудной клетки при больших дефектах межжелудочковой перегородки обнаруживает усиление легочного рисунка, усиленную пульсацию корней легких, увеличение размеров сердца. Зондирование правых полостей сердца выявляет повышение давления в легочной артерии и правом желудочке, возможность проведения катетера в аорту, повышенную оксигенацию венозной крови в правом желудочке. Аортография проводится для исключения сопутствующих ВПС.
Дифференциальная диагностика дефекта межжелудочковой перегородки проводится с открытым атриовентрикулярным каналом, общим артериальным стволом, дефектом аортолегочной перегородки, изолированным стенозом легочной артерии, стенозом аорты, врожденной митральной недостаточностью, тромбоэмболией.
Лечение дефекта межжелудочковой перегородки
Асимптомное течение дефекта межелудочковой перегородки при его небольших размерах позволяет воздержаться от хирургического вмешательства и осуществлять динамическое наблюдение за ребенком. В ряде случаев возможно спонтанное закрытие дефекта межжелудочковой перегородки к 1-4 годам жизни или в более позднем возрасте. В остальных случаях показано хирургическое закрытие дефекта межжелудочковой перегородки, как правило, после достижения ребенком 3-х лет.
При развитии сердечной недостаточности и легочной гипертензии проводится консервативное лечение с помощью сердечных гликозидов, мочегонных препаратов, ингибиторов ангиотензинпревращающего фермента, кардиотрофиков, антиоксидантов.
Кардиохирургическое лечение дефекта межжелудочковой перегородки может быть радикальным и паллиативным. К радикальным операциям относятся ушивание малых дефектов межжелудочковой перегородки П-образными швами; пластика больших дефектов синтетической (тефлон, дакрон и др.) заплатой или биологической (консервированный ксеноперикард, аутоперикард) тканью; рентгенэндоваскулярная окклюзия дефекта межжелудочковой перегородки.
У грудных детей с выраженной гипотрофией, большим лево-правым шунтированием крови и множественными дефектами предпочтение отдается паллиативной операции, направленной на создание искусственного стеноза легочной артерии с помощью манжетки. Данный этап позволяет подготовить ребенка к радикальной операции по устранению дефекта межжелудочковой перегородки в более старшем возрасте.
Течение беременности при дефекте межжелудочковой перегородки
Женщины с небольшим дефектом межжелудочковой перегородки, как правило, в состоянии нормально выносить и родить ребенка. Однако, при больших размерах дефекта, аритмии, сердечной недостаточности или легочной гипертензии риск осложнений во время беременности значительно повышается. Наличие синдрома Эйзенменгера является показанием для искусственного прерывания беременности. У женщин с дефектом межжелудочковой перегородки имеется повышенная вероятность рождения ребенка с аналогичным или другим врожденным пороком сердца.
Перед планированием беременности пациентке с пороком сердца (оперированным или нет) необходимо проконсультироваться с акушером-гинекологом, кардиологом, генетиком. Ведение беременности у категории женщин с дефектом межжелудочковой перегородки требует повышенного внимания.
Прогноз при дефекте межжелудочковой перегородки
Естественное течение дефекта межжелудочковой перегородки в целом не позволяет надеяться на благоприятный прогноз. Продолжительность жизни при данном пороке зависит от величины дефекта и составляет в среднем около 25 лет. При больших и средних дефектах 50-80% детей умирают в возрасте до 6 мес. или 1 года от сердечной недостаточности, застойной пневмонии, бактериального эндокардита, нарушений ритма сердца, тромбоэмболических осложнений.
В редких случаях ДМЖП не оказывает существенного влияния на продолжительность и качество жизни. Спонтанное закрытие дефекта межжелудочковой перегородки наблюдается в 25-40% случаев, преимущественно при его малом размере. Однако даже в этом случае больные должны находиться под наблюдением кардиолога в связи с возможными осложнениями со стороны проводящей системы сердца и высоким риском возникновения инфекционного эндокардита.
Источник
Невозможно описать словами тревогу и растерянность, если вам пришлось столкнуться с таким грозным диагнозом, как врожденный порок развития у малыша. Одна из наиболее часто встречающихся детских сердечных патологий — дефект межжелудочковой перегородки сердца (ДМЖП). Разберем симптомы и признаки, которые позволяют её заподозрить, поговорим о методах диагностики и лечения, попробуем уточнить, можно ли обнаружить этот порок у ребенка внутриутробно — на этапе беременности.
Что это такое
В норме сердечные желудочки разделены мышечной преградой уже к моменту рождения младенца. Она не только составляет треть их общей площади, но и принимает активное участие в каждом сокращении и расслаблении сердца. Органы плода получают лишь смешанную кровь. Оба желудочка новорожденного «заняты работой» примерно одинаково, этим объясняется отсутствие разницы в толщине их мышечных стенок.
Патогенез нарушения кровообращения при ДМЖП
Межжелудочковая перегородка возникает из трех различных структур, формирование её завершается к 4-5 недели беременности. Если срастания не происходит – между желудочками остается отверстие (дефект). Он может оказаться единственной аномалией развития сердца (изолированным пороком) либо сочетаться с другими врожденными изменениями анатомии, входить в структуру комбинированного порока. Сегодня мы говорим лишь о первом варианте.
В первые часы жизни вашего ребенка, после того, как малыш задышал, изменяется вся система его кровотока. Включение большого и малого кругов кровообращения «заставляет» сердце младенца перестроить свою работу:
- Значительно повышается давление в левом желудочке.
- При ДМЖП часть крови попадает не только в аорту, но и в правый желудочек, создавая для последнего дополнительную нагрузку. Специалисты называют этот процесс сбросом крови «слева — направо» (из левой половины сердца – в правую).
- Правый желудочек «вынужден» функционировать интенсивнее, чтобы перекачать «лишнюю» кровь.
Изменения гемодинамики напрямую зависят от величины и локализации дефекта. Отверстие малых размеров может закрыться у ребенка к 4-5 годам жизни самостоятельно (спонтанно). Обычно в 65-75% случаев так и происходит. При обширных дефектах «страдает» не только правый желудочек. Возрастает давление в малом круге кровообращения, возникает легочная гипертензия.
Организм малыша попытается компенсировать нагрузку:
- Увеличивается масса желудочков.
- Утолщаются стенки крупных и мелких артерий.
- Благодаря этим механизмам давление в обоих желудочках сравнивается. Несмотря на имеющееся отверстие, сброса крови какое-то время не происходит.
- Постепенно защитные силы организма истощаются, и давление в правом желудочке становится больше, чем в левом.
- Венозная кровь через дефект начнет поступать в большой круг кровообращения – синдром Эйзенменгера. Возникает декомпенсация порока. Клинически данный процесс проявляется тем, что ребенок начинает «синеть».
К счастью, при ранней диагностике и своевременном оперативном лечении этого не происходит, даже если ДМЖП имеет большие размеры. Поэтому постарайтесь прислушаться к советам своего врача. Конечно, самой лучшей операцией хирурги считают ту, которую больному делать не нужно. Но дефект межжелудочковой перегородки у новорожденного требует тщательного обследования, консультаций специалистов, дифференцированного подхода к ведению пациентов.
Классификация дефектов межжелудочковой перегородки
Согласно Международной классификации болезней 10 пересмотра (МКБ-10), любой ДМЖП кодируется шифром – Q 21.0. Однако в практической педиатрии врачи выделяют четыре анатомических типа данной аномалии, согласно «Клиническим рекомендациям по ведению детей с врожденными пороками сердца», утвержденным Ассоциацией сердечно-сосудистых хирургов в 2013 году:
- Субартериальный дефект межжелудочковой перегородки. Располагается непосредственно под клапаном легочной артерии. Листок аорты может «прогибаться», «вклиниваться» в существующее отверстие, что вызывает аортальную регургитацию (обратный сброс крови).
- Перимембранозный дефект межжелудочковой перегородки – отверстие располагается в мембранной части, прилегающей к трехстворчатому клапану. Мембранозная перегородка может срастаться с дефектом, отчасти прикрывая его.

- Приточный дефект межжелудочковой перегородки – локализуется в приточной части правого желудочка.
- Мышечный дефект межжелудочковой перегородки — может располагаться по центру мышцы, в верхней части, а также — на границе между стенкой правого желудочка и самой перегородкой. Иногда определяются сразу несколько мелких отверстий (множественный тип мышечного ДМЖП – болезнь Толочинова-Роже).
Чтобы вас не пугали медицинские термины, и стало понятно, где именно отверстие в межжелудочковой перегородке у вашего ребенка, попробую объяснить ещё. Анатомы разделяют эту структуру на три части – верхнюю (мембранозную), среднюю (мышечную), нижнюю (трабекулярную). Следовательно, трабекулярный изъян располагается в нижней, мышечный – в средней, мембранозный дефект межжелудочковой перегородки – в верхней её части.
Причины возникновения дефекта
Точную причину возникновения аномалии установить трудно. В этиологии врожденных пороков сердца доказана роль наследственности, загрязненной окружающей среды, вредных привычек родителей, приема будущей мамой некоторых лекарственных препаратов, перенесенных вирусных инфекций во время беременности.
Совет врача
Неоднократно родители терзали себя и меня, пытаясь выяснить точную этиологию врожденного порока у ребенка. Когда такой диагноз обнаруживают у родного малыша, хочется непременно найти виновного. Бабушка с папиной стороны иногда обвиняет невестку в «плохой генетике», мамина родня — зятя в курении и употреблении алкоголя.
Категорически не советую вам этого делать. Конечно же, причину узнать важно для того, чтобы прогнозировать рождение здоровых или больных детей у родителей и самого ребенка. Малыш с ДМЖП когда-нибудь сам станет отцом или матерью. Но болезнь маленького человека – не повод для выяснения отношений. Забудьте семейные ссоры. Сосредоточьтесь на заботе о малютке.
Как заподозрить порок: симптомы и признаки у ребенка
При незначительном размере отверстия ваш малыш ничем не будет отличаться от сверстников. Вероятно, ещё в родильном отделении неонатолог сообщит, что у вашего младенца обнаружен систолический сердечный шум. Родители обычно с тревогой спрашивают при каждой аускультации: «Шум – уменьшился или стал сильнее?» Парадокс ДМЖП в том, что интенсивность шума обратно пропорциональна размерам отверстия. Чем слабее шум – тем больше величина дефекта.
Серьезнее ситуация, если малыш родился «без шума», но:
- с трех-четырехнедельного возраста вдруг перестал набирать вес при достаточном количестве молока у матери;
- у него появилась одышка во время кормления;
- респираторные инфекции «преследуют» его чаще, чем других детей;
- иногда ребенок начинает «синеть»;
- при осмотре врач вдруг обнаруживает расширение границ сердца, увеличение печени.
В дальнейшем клиническая картина характеризуется разлитым усиленным верхушечным толчком, появлением систолического дрожания слева в третьем-четвертом межреберьях, расширением границ сердца, особенно влево, образованием сердечного горба (грудь Девиса).
Методы диагностики
Аускультативные данные и другие симптомы позволят педиатру заподозрить врожденный порок развития у ребенка. Скорее всего, детский кардиолог для уточнения диагноза выпишет направление на:
- Рентгенографию органов грудной клетки – при малом дефекте изменений не обнаружится. Если отверстие значительных размеров, могут выявиться гипертрофия левого предсердия и желудочка, усиление рисунка легких. В случае осложнения ДМЖП легочной гипертензией -выбухание дуги легочной артерии при ослаблении рисунка легких и негипертрофированном левом желудочке.
- Электрокардиографию – в дифференциации порока сердца не имеет особого значения, но позволит выявить отклонение электрической оси, а также признаки перегрузки обоих либо лишь левого желудочка.
- Эхокардиографию – считается главным диагностической технологией при сердечных пороках. Ультразвуковой метод обследования позволяет уточнить точную локализацию отверстия, его размеры, количество дефектов, а также оценить изменения гемодинамики. Основная задача проведения УЗИ – непосредственная визуализация порока, исключение других аномалий сердца. Допплеровское картирование поможет установить величину сброса, наличие регургитации крови, оценить систолическое давление в правом желудочке.
Если на ЭхоКГ дефекты видны недостаточно хорошо, или врач заподозрил комбинированный порок сердца, возможно, понадобится пройти магнитно-резонансную либо компьютерную томографию.
Катетеризация сердца и ангиография
Обычно детям эти диагностические методики назначаются редко, но, если неинвазивные методы не дают полной информации о состоянии, выполняются для оценки гемодинамики в малом круге кровообращения и легочной гипертензии. При данной процедуре измеряется давление в аорте, легочной артерии, определяется газовый состав крови внутри сердечных камер и крупных сосудов. Проводится опытными специалистами в регионарных центрах.
Лечение дефекта межжелудочковой перегородки
Подход к ведению пациентов с ДМЖП строго индивидуальный, зависит от размеров и локализации дефекта, клиники (возникновение легочной гипертензии, развитие недостаточности кровообращения), наличия сопутствующей патологии.
Если отверстие небольшое, нет нарушений гемодинамики, ребенок нуждается лишь в регулярных осмотрах кардиолога и периодическом проведении ЭхоКГ. При малейших сомнениях в благоприятном течении заболевания показано оперативное лечение.
Различают следующие виды хирургической коррекции ДМЖП:
- Операция в условиях искусственного кровообращения, во время которой кардиохирург ушивает отверстие или закрывает его клапаном.
- «Вспомогательное» сужение легочной артерии – предварительная хирургическая подготовительная операция для предотвращения декомпенсации порока. Позволяет «выиграть время» до радикальной коррекции.
- Малоинвазивное эндоваскулярное вмешательство. Проводится под контролем УЗИ и рентгеноскопии. Через бедренную артерию сосудистый хирург вводит специальное устройство (спираль либо окклюдер), проведя его в полость сердца, закрывает дефект.
- Гибридная операция. После вскрытия грудной клетки вводится окклюдер непосредственно через прокол миокарда. Протокол вмешательства не предусматривает остановки сердца и подключения его к системе искусственного кровообращения.
Какой метод наиболее подойдет вашему ребенку – решает специалист. Без письменного согласия родителей на оперативное вмешательство ни один врач малыша оперировать не будет. Важно обсудить с врачом ход операции, выбрав наиболее оптимальную тактику.

Следует помнить, что, если упустить драгоценное время, не закрыть отверстие до развития легочной гипертензии, существует риск смерти от недостаточности кровообращения. Медикаментозную терапию назначают как подготовку к хирургическому вмешательству, в период реабилитации, а также при развитии декомпенсации порока с целью поддержать работу сердца.
Каков прогноз и будет ли здоров ребенок
Прогноз заболевания во многом зависит не только от вида дефекта, но и от своевременного оперативного вмешательства. Никогда не забуду одну семью. Вера родителей не позволяла им предохраняться от беременности. Чудесная девочка родилась восьмым ребенком по счету. Все старшие дети – абсолютно здоровы. Никаких факторов риска. Прекрасная наследственность. Отличный вес и показатели по Апгар. Малышка брала грудь, была активна и являлась всеобщей любимицей.
Случай из практики
В родильном отделении неонатолог заподозрила врожденную патологию сердца. Ультразвуковое обследование выявило мышечный дефект межжелудочковой перегородки у новорожденной. Специалисты кардиоцентра рекомендовали провести оперативную коррекцию до 6-месячного возраста, так как размер отверстия оказался слишком велик.
Родители настроились на хирургическое лечение, но, согласно их вере, требовалось благословение пастора. А тот, увидев вполне с виду здоровую девочку, посоветовал немного повременить с операцией. Мол, она ещё совсем маленькая, порок её не беспокоит, «разрезать» всегда успеете.
На седьмом месяце жизни у малышки появились первые признаки легочной гипертензии, с которой мы пытались безуспешно бороться назначением медикаментов. На девятом — родители умоляли кардиохирургов спасти ребенка, но оперировать было поздно — развилась клиника сердечной недостаточности. В годик девочка умерла.
А вчера на прием пришел юноша. Восемнадцать лет. Возмущался, что врачи призывной комиссии его отправили на дополнительное обследование в больницу. Занимается легкой атлетикой. Мечтает поступить в военное училище. Открываю амбулаторную карту, а там – оперативное лечение по поводу ДМЖП. На груди – тонюсенькая полоска послеоперационного шрама, практически незаметная. Парень операции не помнит. Искренне не понимает, чем он болен. Просто родители в свое время не побоялись его «разрезать».
Можно ли диагностировать дефект до рождения ребенка
Да, можно. Для этого необходимо своевременно пройти ультразвуковое обследование во время беременности у опытного специалиста на современном оборудовании. Если у будущего малыша подозрение на ДМЖП — постарайтесь выбрать роддом поближе к кардиоцентру.
Нередко приходится слышать упреки родителей, что они выполняли все рекомендации врачей, но порок сердца был выявлен лишь после рождения ребенка. К сожалению, отверстие межжелудочковой перегородки диаметром до 4мм очень трудно обнаружить без цветового допплеровского картирования. Поэтому, если у вас отягощенная наследственность, вы курили до наступления беременности, переболели гриппом или ОРВИ, когда ожидали малыша, – обязательно сообщите об этом вашему гинекологу. Возможно, понадобится пройти дополнительное УЗИ на более чувствительном оборудовании.
Источник
