Противопоказания для лучевой терапии головного мозга

Показания к лучевой терапии злокачественных опухолей. В настоящее время показания к лучевому лечению злокачественных опухолей достаточно широки – 65-70% онкологических больных как в неоперабельной, так и в операбельной стадиях заболевания подлежат такому лечению.
Показания к лучевой терапии определяются на основании всесторонней оценки состояния органов и систем больного и характеристики выявленного опухолевого поражения. Поэтому с помощью клинических, лучевых, инструментальных и лабораторных методов определяют состояние органов и систем больного, локализацию и характер роста опухолей, стадию ее развития. Там, где это возможно, стадию устанавливают по системе TNM, где Т – параметры опухоли, N – наличие или отсутствие вовлечения лимфоузлов, а М – наличие или отсутствие отдаленных метастазов. Требуется морфологическое подтверждение клинического диагноза посредством биопсии, цитологического изучения пунктатов или смывов. Главной стратегической основой успешности хирургического, лучевого и медикаментозного лечения является ранняя диагностика опухолевого процесса. В онкологической клинике применяют три основных (специальных) варианта лечения больного: хирургический, лучевой и химиотерапевтический. План лечения определяется консилиумом в составе: хирурга (онколога), лучевого терапевта и химиотерапевта, а также других специалистов в зависимости от клинической ситуации.
Противопоказания к лучевой терапии:
1. Распад опухоли с нагноением и/или кровотечением.
2. Прорастание в полые органы.
3. Наличие отдаленных (особенно множественных) метастазов.
4. Общее тяжелое состояние больного за счет интоксикации.
5. Кахексия.
6. Выраженная анемия, лейкопения, тромбоцитопения.
7. Септические заболевания, активный туберкулез легких.
8. Недавно перенесенный инфаркт миокарда (менее года назад).
9. Декомпенсация кровообращения, функции печени и почек.
Варианты лучевой терапии
Лучевая терапия как самостоятельный метод лечения может быть проведена по радикальной программе, использована как паллиативное и симптоматическое средство помощи больным.
Радикальная лучевая терапия направлена на полное излечение больного от опухоли и регионарных метастазов путем подведения канцерицидной дозы радиации. Уровни канцерицидных доз для различных опухолей неодинаковы и устанавливаются в зависимости от гистологического ее строения, митотической активности и степени дифференцировки клеточных элементов. К числу опухолей, поддающихся радикальному лечению (радиокурабельные опухоли), относят рак кожи, губы, носоглотки, гортани, молочной железы, шейки матки и эндометрия, предстательной железы, а также семиномы, локализованные лимфомы, лимфогранулематоз, аденомы гипофиза. Понятно, успех может быть достигнут на относительно ранних стадиях.
Паллиативная лучевая терапия предпринимается для уменьшения размеров опухоли и ее метастазов, стабилизации опухолевого роста и используется в тех случаях, когда невозможна лучевая терапия по радикальной программе, при этом суммарная очаговая доза (СОД), как правило, составляет 2/3 канцерицидной.
Симптоматическая лучевая терапия применяется для снятия или уменьшения клинических симптомов злокачественного поражения, могущих привести к быстрой гибели больного или существенно ухудшающих качество его жизни. Облучение с симптоматической целью проводится по жизненным показаниям при опухолях таких локализаций, при которых лучевая терапия – единственный метод лечения (синдром сдавления верхней полой вены, компрессионный синдром, обусловленный быстрорастущей опухолью мозга, острая асфиксия при быстрорастущей опухоли трахеи, первичные и метастатические опухоли, вызывающие сдавление спинного мозга). Суммарная поглощенная доза излучения устанавливается индивидуально, в зависимости от достигнутого эффекта.
Комбинированное лечение. Этот термин используется, когда в той или иной последовательности для специального лечения злокачественных опухолей применяется оперативное лечение и лучевая терапия. Лучевая терапия в комбинации с хирургическим вмешательством может быть использована в предоперационном периоде, после операции и интраоперационно.
Предоперационное облучение проводится с целью улучшения условий выполнения радикальной операции и снижения частоты развития местных рецидивов и отдаленных метастазов. Задачи предоперационной лучевой терапии:
Разрушение наиболее радиочувствительных клеток и понижение жизнеспособности оставшихся опухолевых элементов;
Устранение воспалительных явлений в опухоли и вокруг нее;
Стимуляция и развитие соединительной ткани и инкапсуляция отдельных комплексов раковых клеток;
Облитерация мелких сосудов, ведущая к понижению васкуляризации стромы опухоли и тем самым к уменьшению опасности метастазирования;
Перевод опухолей в операбельное состояние.
Многолетний опыт проведения комбинированного лечения показывает, что очаговая доза не более 40 Гр, подводимая по 2 Гр ежедневно в течение 4 недель, не вызывает затруднений при выполнении последующей операции и не оказывает заметного влияния на заживление послеоперационной раны. То же можно сказать и о других режимах фракционирования по биологическому эффекту эквивалентных 40 Гр обычным фракционированием (25 Гр за 5 фракций). Доза 40-45 Гр приводит к гибели 90-95% субклинических очагов опухолевого роста. Превышение дозы 40-45 Гр, хотя и желательно для усиления повреждающего эффекта на опухолевые клетки, но может увеличить частоту послеоперационных осложнений. В настоящее время наиболее часто используют две методики предоперационного дистанционного облучения:
1. ежедневное облучение первичной опухоли и регионарных зон в дозе 2 Гр до СОД 40-45 Гр за 4-4,5 недели лечения;
2. облучение аналогичных объемов в дозе 5 Гр в течение 5 дней до СОД 25 Гр.
В первом варианте операцию выполняют через 2-3 недели, а во втором – не позднее 1-3 дней; она рекомендуется только для лечения больных с операбельными злокачественными опухолями.
Послеоперационная лучевая терапия имеет цель: увеличить эффективность операции с помощью лучевого воздействия на оставленные или имплантированные во время хирургического лечения (вмешательства) опухолевые элементы. Послеоперационное облучение, как и предоперационное, в конечном итоге, направлено на предупреждение рецидивов и уменьшение метастазирования злокачественной опухоли. Ее задачи:
1. “стерилизация” операционного поля от рассеянных в процессе оперативного вмешательства злокачественных клеток и их комплексов;
2. эрадикация оставшихся злокачественных тканей после неполного удаления опухоли и метастазов.
Показания к проведению послеоперационного облучения: в случаях, когда оперативное вмешательство радикально выполнить невозможно (опухоли ЦНС, ротоглотки, забрюшинного пространства), выход опухоли за пределы того слоя, в котором она возникла, распространение по лимфатической системе, органосохраняющие операции.
Следует заметить, что послеоперационное облучение проводится в условиях, способствующих повышению радиорезистентности опухолевых клеток (из-за нарушения крово- и лимфообращения). Одновременно радиочувствительность нормальных тканей в состоянии регенерации повышается. Все это приводит к уменьшению радиотерапевтического интервала. Однако можно отметить определенные достоинства послеоперационной лучевой терапии:
1. выбор объема и методики облучения проводят на основании данных, полученных во время операции и после тщательного морфологического изучения удаленных тканей;
2. оперативное лечение выполняют максимально быстро, после уточняющей диагностики.
Послеоперационное облучение проводят при условии полного заживления послеоперационной раны, через 2-3 недели после операции. Облучают обычными фракциями в СОД 50 Гр при отсутствии злокачественных клеток в операционных разрезах, при их наличии – 60 Гр.
Интраоперационная лучевая терапия предусматривает однократное облучение операционного поля или неоперабельных опухолей во время лапаротомии электронным пучком с энергией 10-15 МэВ в дозе 14-20 Гр.
Комплексная лучевая терапия предусматривает сочетанное использование лучевой и химиотерапии и преследует двоякую цель: взаимное усиление воздействия ионизирующей радиации и химиотерапии на первичную опухоль (достижение аддитивного, потенцирующего и синхронизирующего эффектов), а также создание условий для профилактики метастазов и лечения субклинических или же выявленных метастазов. Различают два основных варианта комплексного лечения:
1. когда лучевая терапия – основной, или базовый, метод, а химио-гормональное лечение – дополнительный, направленный на излечение отдаленных метастазов, при этом подводится СОД не ниже 60 Гр.
Так, при комплексном лечении больных инфильтративно-отечными формами рака молочной железы облучение проводят в дозах не менее 60 Гр на молочную железу, 55-60 Гр на зоны регионарного метастазирования. Адъювантная химиогормонотерапия направлена на эрадикацию возможных субклинических отдаленных метастазов и в меньшей степени на повреждение первичного очага в молочной железе (это относится и к немелкоклеточному раку легкого, головы, шеи, пищевода, эндометрия и т.д.).
2. когда ионизирующее излучение используется как адъювантное средство химиолучевого лечения. В этих случаях дозы облучения могут быть уменьшены на 1/3 от “канцерицидной” и составляют 30-36 Гр. Применяется при лечении опухолей яичка, нефробластомах, лимфогранулематозе, злокачественных неходжкинских лимфомах.
Используется, как правило, вариант обычного фракционирования дозы, т.к. возможен синергизм и в отношении поражения здоровых тканей. Последовательность может варьировать в зависимости от конкретной локализации.
Мультимодальная терапия онкологических больных предусматривает оптимальное использование современных методов хирургического, лучевого и лекарственного лечения, а также сочетание их с радиомодифицирующими воздействиями.
Принципы лучевой терапии злокачественных опухолей:
1. Максимальное лучевое воздействие на опухолевую ткань, минимальное – на здоровую ткань.
2. Эффективность лучевого лечения в решающей степени зависит от стадии заболевания, поэтому облучение следует начинать как можно раньше.
3. Для достижения благоприятного конечного результата важно добиваться максимальной радикальности первого курса лучевого лечения, что достигается обязательным облучением всей опухоли в необходимой дозе и в оптимальные сроки.
4. Под необходимой дозой понимают такую, которая достаточна для получения запланированного эффекта при учете величины опухоли, характера ее роста (преобладание экспансивного или инфильтративного роста), радиочувствительности опухолевой ткани и некоторых других факторов. Необходимая суммарная очаговая доза при лечении по радикальной программе 60-80 Гр должна быть получена всем опухолевым узлом, тогда как на пути лимфооттока и на зоны регионарного метастазирования достаточной является доза, составляющая около 80% очаговой (при отсутствии в них метастазов).
5. Под оптимальными сроками облучения понимают такую общую продолжительность лечения и распределения дозы во времени (т.е. способы фракционирования), при которых достигается существенное подавление опухолевого роста при сохранении достаточной степени регенераторных способностей окружающих опухоль здоровых тканей. Таким образом, облучение в оптимальные сроки является одним из важных условий поддержания максимальной величины радиотерапевтического интервала (различие в радиопоражаемости опухоли и окружающих здоровых тканей), что, в свою очередь, в значительной степени определяет результаты лечения.
6. Сохранению и увеличению радиотерапевтического интервала способствуют, помимо распределения дозы во времени, воздействие на радиочувствительность опухолевой ткани путем применения радиопротекторов и радиосенсибилизаторов, а также использование таких видов излучений и таких методик облучения, которые обеспечивают наилучшее распределение дозы.
7. Эффективность лучевого лечения в значительной степени зависит от своевременности применения патогенетически обоснованного сопутствующего лечения, направленного на дезинтоксикацию и нормализацию функций организма облученного пациента, снятие воспалительного процесса в зоне облучения и предупреждение возникновения лучевых реакций и повреждений. Сопутствующее лечение включает психологическую подготовку, режим питания с использованием радиопротекторных свойств пищи, витаминотерапию, гемотрансфузию, лекарственное лечение, лечебную физкультуру, уход за кожей.
Клинико-дозиметрическое планирование лучевой терапии
Основной принцип лучевой терапии – излечение опухоли при максимальном щажении нормальных органов и тканей. Для реализации его в клинике большое внимание уделяется разработке способов повышения эффективности лучевого воздействия на основе пространственного и временного распределения дозы ионизирующего излучения и применения средств, изменяющих (модифицирующих) лучевые реакции опухоли и организма.
Цель планирования лучевой терапии – включение в зону облучения минимально возможного объема тканей, но в то же время достаточного для воздействия на все опухолевые элементы. Исходя из этого, различают 5 типов объемов облучения. Большой (макроскопический) объем опухоли (БОО) включает видимую опухоль. Клинический объем мишени (КОМ) включает видимую опухоль и объемы предполагаемого субклинического распространения. Концепция КОМ является клинико-анатомической. Планируемый объем мишени (ПОМ) включает КОМ и окружающие ткани с поправкой на вариации в размере, форме и положении относительно лечебных пучков, поэтому ПОМ является геометрической концепцией. Объем, который получает дозу, достаточную для радикального или паллиативного лечения с учетом толерантности нормальных тканей, обозначается как объем лечения. Наиболее оптимальное распределение дозы излучения достигается при объемном (трехмерном) планировании. Объемное планирование лежит в основе конформного облучения, при котором во время перемещения пучка излучения поле облучения регулируется по форме и размерам в соответствии с изменением поперечного сечения мишени, перпендикулярного направлению пучка в пространстве.
Служба предлучевой подготовки предназначена для проведения комплексной топометрии больных, подлежащих различным видам лучевой терапии с использованием биометрических, рентгенологических, изотопных, УЗ и МРТ методов исследования, для клинико-дозиметрического обеспечения курса лучевой терапии.
Предлучевая подготовка и клиническая топометрия. Основой лучевого лечения онкологических больных является правильное подведение заданной дозы к злокачественному очагу при минимальном облучении окружающих его здоровых органов и тканей. Определение размеров, площади, объема патологических образований, органов и анатомических структур, описание в количественных терминах их взаимного расположения (синтопии) у конкретного больного называется клинической топометрией. Для того, чтобы выбрать варианты и параметры программы облучения, нужно знать форму и размеры очага-мишени, ее ориентацию в теле пациента, а также синтопию окружающих органов и тканей, расстояние между мишенью и наиболее важными, с точки зрения распределения лучевой нагрузки, анатомическими структурами и «критическими органами». Эти сведения позволяют получить различные методы лучевой диагностики, но наиболее часто применяется для этих целей рентгеновская компьютерная томография. Данные, полученные при выполнении оперативных вмешательств, также позволяют определить размеры опухоли. Затем изготавливают схемы сечения тела на уровне “мишени”– так называемые топометрические схемы (т.е. производят клиническую топометрию). Современные системы дозиметрического планирования воспринимают топометрическую информацию непосредственно с магнитного носителя КТ и печатают топометрическую карту с нанесенным на ней выбранным распределением изодоз. Изодозные линии соединяют точки с одинаковым значением поглощенной дозы. Отмечают относительные значения – в процентах от максимальной поглощенной дозы, принимаемой за 100%. Для расчета изодозных кривых используются специальные компьютерные программы, которые учитывают пространственные параметры облучаемого объекта и дозиметрическую характеристику применяемого пучка излучения. Для того, чтобы составить представление о распределении поглощенных доз в облучаемом объеме, на топометрические схемы наносят изодозные кривые и получают, таким образом, карту изодоз. В практике лучевой терапии дозное распределение считают приемлемым, если вся опухоль заключается в дозе 100-90%, зона субклинического распространения опухоли и регионарного метастазирования находится в пределах 80% изодозы, а здоровые ткани – не более 50-30% изодозы.
Источник
Специалисты отделения опухолей головы и шеи НМИЦ онкологии имени Н.Н. Петрова подготовили ответы на самые частые вопросы пациентов, проходящих лучевую терапию. Они рассказали, с какими побочными эффектами можно столкнуться во время этого длительного и непростого лечения, как их избежать или облегчить.
Что такое лучевая терапия? В каком случае она назначается?
Лучевая терапия (радиотерапия, облучение) — современный метод лечения с помощью ионизирующего излучения. В качестве ионизирующего излучения в зависимости от видов и задач лучевой терапии могут быть использованы разные виды лучей (рентгеновские или гамма-лучи). Они вызывают сходные биологические эффекты в клетках и тканях, определяя лечебное действие облучения.

Количество полученного облучения называется дозой и измеряется в греях (Гр). Доза облучения при разных типах лучевой терапии назначается индивидуально с учётом многих факторов — особенностей как самого заболевания (вид, стадия, локализация), так и пациента.
Лучевая терапия проводится только при наличии показаний в результате взвешенного решения. При этом специалисты всегда руководствуются важной целью — оказать наилучшую помощь пациенту в лечении его заболевания. Обязательно оцениваются риски и выгоды, устанавливается соотношение пользы и вреда от облучения.
Всегда ли возникают осложнения?
Многие пациенты волнуются, ожидая тяжёлых осложнений от лучевого лечения. Следует помнить, что каждый человек — индивидуален. Нежелательные эффекты могут быть почти незаметными или временными, не все из них будут у конкретного пациента.
Но надо помнить, что как у любого метода лечения, у лучевой терапии есть побочные эффекты. Большинство из них возникает постепенно обычно к концу второй недели облучения. Они делятся на ранние лучевые реакции и поздние лучевые реакции, проявляются в органах, расположенных непосредственно в поле облучения.
Во время лечения могут проявиться тошнота, снижение аппетита, покраснения на коже, потеря концентрации внимания, выпадение волос, слабость и прочее.
Какие осложнения при проведении лучевой терапии у пациентов с опухолями головы и шеи бывают и как с ними справиться?
Проблемы с питанием и потеря веса
Для успешного прохождения лечения необходимо качественно и сбалансировано питаться. Лечение – не время диет для похудения. В этот период организм нуждается в дополнительной энергии для борьбы с болезнью. К сожалению, именно в этот момент возникают побочные эффекты, из-за которых принимать достаточное количество пищи не получается, что и ведёт к потере веса и нарушению работы всех органов и систем организма.
В далеко зашедших случаях приходится прерывать лучевую терапию. Поэтому пациенту необходимо очень внимательно отнестись к своему рациону, количеству и качеству съедаемой пищи в день.
Какие проблемы могут возникать?
Они разные, но встречаются почти у всех:
- снижение или потеря аппетита,
- нарушение вкусовых ощущений и запаха,
- сухость во рту,
- тошнота,
- нарушение глотания,
- боль в ротовой полости.
Что может помочь?
Принимайте пищу дробно. По 6-8 раз в день. Порции должны быть небольшие, а еда негорячая.
Не допускайте длительных перерывов без пищи. Всегда имейте под рукой то, чем можно перекусить.
Не ешьте бесполезной, пустой еды. Каждый кусочек должен нести пользу. Выбирайте высококалорийные продукты, богатые белком.

Переходите на мягкую или измельчённую пищу. Можно самостоятельно использовать блендер.
Не отчаивайтесь, если любимое блюдо перестало быть вкусным, ищите альтернативные варианты. Это временное явление, после лечения вкус еды постепенно вернётся.
Пейте достаточное количество жидкости.
Контролируйте свой вес: взвешивайтесь каждые два дня.
Не употребляйте алкоголь, он раздражает и дополнительно сушит слизистую рта. Алкоголь оказывает общее токсическое действие на организм.
Каждый день необходимо наблюдать за собой. Если наступает момент, когда количество потребляемой пищи и жидкости заметно уменьшилось, а вышеперечисленные советы не помогают, не надо скрывать это от лечащего врача.
В этом случае он назначит дополнительно специализированное питание и инфузионную терапию.
В некоторых ситуациях лечащий врач принимает решение установить назогастральный зонд, и тогда питание происходит через него, а ротовая полость изолируется от контакта с пищей, это даёт возможность сохранить целостность слизистых оболочек в ротовой полости, не происходит травматизация обожжённых тканей. Многие пациенты боятся и всячески избегают этой процедуры, но, по отзывам тех, кому пришлось с этим столкнуться, зонд — это спасение. Как, чем и в каком режиме питаться через зонд обучает медицинская сестра стационара, где пациент проходит лечение.
В некоторых ситуациях пациентам показано формирование гастростомы: при обширном распространении опухоли на шее, при невозможности питаться, когда пища совсем не проходит. Гастростома чаще всего устанавливается эндоскопически, что позволяет избежать травматизации и своевременно начать питание.
Трудности с дыханием
В некоторых ситуациях у пациентов возникает необходимость формирования превентивной трахеостомы. Она нужна в случае, когда пациенту трудно дышать из-за опухоли в области шеи и в ситуации, когда врач понимает, что во время лучевой терапии возникнет отёк мягких тканей, который может привести к удушью.
Боль
Одна из частых проблем — это воспалительное или язвенное поражение ротовой полости и, связанная с этим осложнением, боль.
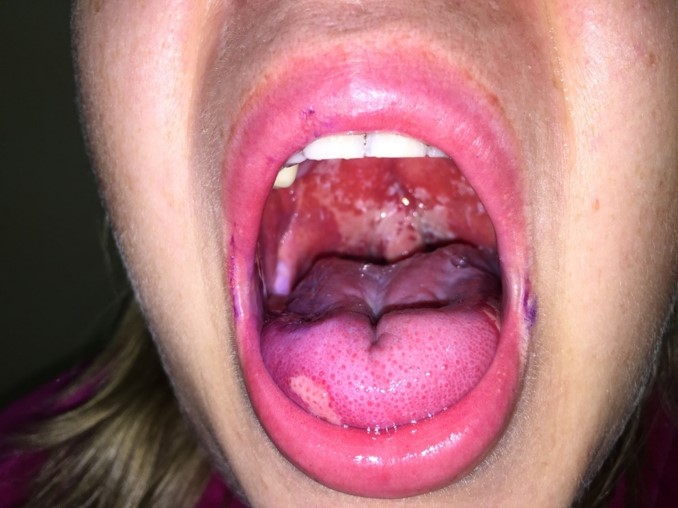
Пациент может заметить уменьшение слюноотделения, изменение вкуса, боль (она может быть острой), жжение, язвочки на слизистой полости рта, затруднение в приёме пищи и глотании.
С самого начала лечения рекомендуется соблюдать тщательную гигиену полости рта:
- использовать мягкую зубную щётку,
- чистить зубы после каждого приёма пищи,
- полоскать ротовую полость физиологическим раствором или другими растворами по назначению врача.
- Необходимо избегать приёма горячей, кислой, раздражающей, грубой пищи, а также горячих напитков.
При развитии вышеперечисленных симптомов лечащий врач назначает соответствующую терапию, в том числе противоболевую, облегчающую возникшее осложнение.
Осложнения со стороны ЖКТ
Запоры являются частой проблемой во время лечения. Причинами могут быть снижение двигательной активности, изменение рациона. Стул должен быть регулярным, ежедневным или через день. При задержке до трёх дней об этом необходимо сообщить врачу.
Диарея — это также осложнение от лечения, о ней обязательно нужно сообщить врачу. Последствия от потери жидкости в организме во время лечения могут быть невосполнимыми, а осложнения очень серьёзными.
Кожные осложнения
Кожные реакции в зоне облучения беспокоят многих пациентов. Лечащий врач назначит специальные средства для ухода за кожей.
Общие рекомендации:
- используйте мягкие, щадящие моющие средства для ежедневной гигиены;
- исключайте любое раздражение: воротнички, украшения, мочалки;
- после умывания высушивайте кожу промакивающими движениями;
- носите одежду с мягкой, свободной горловиной;
- закрывайте кожу от прямых солнечных лучей, используйте солнцезащитные средства SPF50;
- увлажняйте кожу и наносите кремы после сеанса радиотерапии.
Выпадение волос
Выпадение волос — неприятное осложнение, настигающее часть пациентов в процессе лечения.

Общие рекомендации: если выпадение сильное, то необходимо сбрить волосы полностью в парикмахерской. Волосы отрастут. Во время лечения необходимо избегать окрашивания и осветления волос. Для психологического комфорта можно использовать парики, шарфы, банданы или шапочки.
Это наиболее частые проблемы, с которыми может столкнуться пациент, а также способы их решения.
Вот ещё несколько советов, основанных на опыте сопровождения пациентов.
Сопутствующие хронические заболевания. Как их контролировать во время лучевого лечения?
Если у пациента есть хроническое заболевание: гипертония, сахарный диабет, гастрит и т.д., то следует знать, что возможно обострение или изменение его течения. Это может потребовать коррекции дозы принимаемых препаратов. Необходимо быть внимательным к своему самочувствию, аккуратно принимать назначенные лекарства.
Обо всех изменениях своего самочувствия необходимо сообщать лечащему врачу или медицинской сестре.
Что делать курильщикам?
Бесспорно — курение вредно. Необходимо постараться снизить количество выкуриваемых сигарет, а лучше совсем перестать курить.
Полезны ли физические нагрузки во время лечения?
Физические нагрузки должны быть лёгкими и неутомительными. Прогулки полезны и желательны.
Бег, поднятие тяжестей необходимо отложить на потом.
Если у пациента есть хобби: вязание, вышивка, рисование, то желательно взять всё необходимое этих занятий с собой в стационар. Если увлечения нет, то, может быть, стоит попробовать?
Общение, или где найти единомышленников?
Многие согласятся, что очень важно иметь единомышленников, с которыми можно поговорить и обсудить насущные проблемы. В ситуации заболевания единомышленник — это сосед по палате или отделению. Общение, поддержка друг друга, обмен информацией и даже взаимоконтроль помогают лучше и легче перенести лечение. Это доказано опытом.
С другой стороны, соседи по палате могут создавать и проблемы, например, храп! Не стоит пренебрегать берушами для сна. Качественный сон очень важен.

Врачи, медсёстры и другие медицинские работники — это тоже единомышленники пациента. Они рядом и готовы помочь.
Очень важно не замыкаться и не закрываться от окружающего мира.
А если нужна психологическая помощь?
Во многих стационарах есть возможность получить помощь медицинского психолога. Не стоит отказываться, если в этом есть необходимость.
Полезно задать психологу вопросы, которые беспокоят, получить на них ответы и профессиональную психологическую поддержку.
Перед выпиской важно обдумать и записать возникшие вопросы по питанию, обезболиванию, дальнейшему лечению и задать их лечащему врачу. Выписываясь из стационара, пациент должен знать, что ему делать, куда обращаться в той или иной ситуации.
И в завершение пожелание от одного из пациентов НМИЦ онкологии им. Н.Н. Петрова:
«Не терзай себя: «Что теперь будет?», «А в Интернете написано…». Полностью доверься врачу. Сейчас врач – рука Судьбы. Он знает, что делать. Лечение – это просто тяжёлая работа, в которой ты только исполнитель. Исполняй. И не думай. Мысли свои направь на что-нибудь другое – начни разрабатывать новую теорию возникновения Вселенной. Не вызывай жалость к себе у себя самого, и не буди жалость к себе у других. Сам поддерживай своих близких, которые больше чем ты переживают за тебя, это придаст тебе силы. Удачи тебе!»
Пациент Ю. Д.
2013 год, 58 лет, диагноз рак горла IV стадия. В течение 7 месяцев 6 курсов химиотерапии, 33 сеанса лучевой терапии, не прекращая основной работы, переведя её в дистанционную форму.
2020 год, 65 лет. Работа, хобби.
Авторы:

Медсестринский состав отделения ОГШ
- Ольга Сергеевна Корнеева;
- Наталия Сергеевна Василькова;
- Елена Николаевна Степанова;
- Кабанова Лариса Валерьевна;
- Норочевская Инга Васильевна;
- Полякова Оксана Николаевна;
- Игнашова Надежда Борисовна;
- Верюжская Любовь Николаевна.
Источник
