Противопоказания для оперативного вмешательства

Показания к операции разделяют на абсолютные и относительные.
Абсолютными показаниями к операции считают заболевания и состояния, представляющие угрозу жизни больного, которые можно ликвидировать только хирургическим путём.
Абсолютные показания к выполнению экстренных операций иначе называют «жизненными». К этой группе показаний относят асфиксию, кровотечение любой этиологии, острые заболевания органов брюшной полости (острый аппендицит, острый холецистит, острый панкреатит, перфоративную язву желудка и двенадцатиперстной кишки, острую кишечную непроходимость, ущемлённую грыжу), острые гнойные хирургические заболевания (абсцесс, флегмону, остеомиелит, мастит и пр.).
В плановой хирургии показания к операции также могут быть абсолютными. При этом обычно выполняют срочные операции, не откладывая их больше чем на 1-2 нед.
Абсолютными показаниями к плановой операции считают следующие заболевания:
– злокачественные новообразования (рак лёгкого, желудка, молочной железы, щитовидной железы, толстой кишки и пр.);
– стеноз пищевода, выходного отдела желудка;
– механическая желтуха и др.
Относительные показания к операции включают две группы заболеваний:
– Заболевания, которые могут быть излечены только хирургическим методом, но не угрожающие непосредственно жизни больного (варикозное расширение подкожных вен нижних конечностей, неущемлённые грыжи живота, доброкачественные опухоли, желчнокаменная болезнь и др.).
– Заболевания, достаточно серьёзные, лечение которых принципиально можно осуществлять как хирургически, так и консервативно (ишемическая болезнь сердца, облитерирующие заболевания сосудов нижних конечностей, язвенная болезнь желудка и двенадцатиперстной кишки и др.). В этом случае выбор делают на основании дополнительных данных с учётом возможной эффективности хирургического или консервативного метода у конкретного больного. По относительным показаниям операции выполняют в плановом порядке при соблюдении оптимальных условий.
Существует классическое разделение противопоказаний на абсолютные и относительные.
К абсолютным противопоказаниям относят состояние шока (кроме геморрагического шока при продолжающемся кровотечении), а также острую стадию инфаркта миокарда или нарушения мозгового кровообращения (инсульта). Следует отметить, что в настоящее время при наличии жизненных показаний возможно выполнение операций и на фоне инфаркта миокарда или инсульта, а также при шоке после стабилизации гемодинамики. Поэтому выделение абсолютных противопоказаний в настоящее время не имеет принципиально решающего значения.
К относительным противопоказаниямотносят любое сопутствующее заболевание. Однако их влияние на переносимость операции различно.
Наибольшую опасность представляет наличие следующих заболеваний и состояний:
– Сердечно-сосудистая система: гипертоническая болезнь, ишемическая болезнь сердца, сердечная недостаточность, аритмии, варикозное расширение вен, тромбозы.
– Дыхательная система: курение, бронхиальная астма, хронический бронхит, эмфизема лёгких, дыхательная недостаточность.
– Почки: хронические пиелонефрит и гломерулонефрит, хроническая почечная недостаточность, особенно с выраженным снижением клубочковой фильтрации.
– Печень: острый и хронический гепатиты, цирроз печени, печёночная недостаточность.
– Система крови: анемия, лейкозы, изменения со стороны свёртывающей системы. Ожирение. Сахарный диабет.
Источник
Общие требования к хирургическим вмешательствам (операциям)1. Основные предоперационные исследования. Перед любой хирургической операцией должны быть проведены следующие исследования: 2. Абсолютные противопоказания к операции: 3. Относительные противопоказания к операции. Относительные противопоказания возникают при несоответствии между необходимостью хирургического лечения, вызванной заболеванием, объемом предполагаемой операции и риском невмешательства. Это несоответствие во многом определяется местными и временными факторами. Противопоказания, относящиеся исключительно к видеоассистированным эндоскопическим операциям, постоянно пересматриваются. В отношении онкологических операций и вмешательств при септических состояниях необходима дополнительная сдержанность. 4. Общая информация о пациенте и согласие: а) Информация о ходе лечения: продолжительность госпитализации, необходимость в интенсивной терапии, дренажи, необходимость в активном сотрудничестве при физиотерапии, дыхательные упражнения и т.п. б) Отказ от некоторых вредных привычек в период госпитализации, особенно от курения (если необходимо, внесите запись в историю болезни или в форму согласия). в) Общие сведения о пациенте и согласии на операцию:
5. Операционные стандарты: а) Предоперационные: б) Интраоперационные: в) Послеоперационные: 6. Лапароскопические операции: Для экспозиции боковых областей брюшной полости также требуются соответствующие положения. В ходе операции бывает необходимо несколько раз изменить положение пациента, что требует его стабильной фиксации на операционном столе. – Также рекомендуем “Как правильно держать и использовать скальпель?” Оглавление темы “Советы молодым хирургам”:
|
Источник
Уважаемые коллеги.
Я работаю неврологом-консультантом в многопрофильном стационаре хирургической направленности. И главный вопрос, помимо исключения острой неврологической патологии, который передо мною ставится коллегами-хирургами – это вопрос противопоказаний к операции (например, полостной) у пожилых больных с сосудистым анамнезом.
Я недавно закончил специализацию, опыта и знаний объективно маловато, но меня учили не лезть в дебри противопоказаний, ставить свой диагноз, а там пусть хирурги с анестезиологами думают – брать на стол или не брать.
Но в настоящее время коллеги спрашивают напрямую – можно брать, выдержит операцию по цереброваскулярам и т.п.
В принципе, есть возможность выполнять КТ, а также УЗДГ в т.ч. в триплексном режиме.
Соответственно, вопрос: какова должна быть моя тактика и каковы ориентиры? Есть ли критерии/рекомендации/прочее, которые регламентируют данный вопрос? Например, что больного с таким-то стенозом (симптомным, асимптомным) от стольки-то процентов нельзя брать на плановую операцию? И насколько обоснован практически рутинный скрининг у пожилых больных, тем более с соответствующим анамнезом (аморфными “микроинсультами” и т.п.)
P.S. Сильно не бейте, готов учиться 🙂
Но в настоящее время коллеги спрашивают напрямую – можно брать, выдержит операцию по цереброваскулярам и т.п.
Решительно не отвечайте на этот вопрос. Анестезиологи Вам хотят сесть на шею и ножки свесить. Они пытаются перевести на Вас часть своей ответственности, чтобы в случае развития осложнений потом развести руками : “невролог разрешил” ..
То, “выдержит ли больной операцию по цереброваскулярам”, будет зависеть от многих факторов, и в немалой степени, от выбранной анестезиологом тактики. Следует учитывать, что во время операции нередко случается гипотензия и гиповолемия. Насколько они будут критичны для церебральной перфузии, вопрос в принципе малопрогнозируемый. Так что, имхо, пишите, как и прежде, свой осмотр и диагноз, а вопрос о возможности проведения анестезии и оперативного вмешательства пусть решают анестезиолог с хирургом.
То есть, уточню исключительно для себя и своей совести: не существует ориентиров и положений, что, к примеру, больной, перенесший несколько лет назад ОНМК (или даже два) в каротидном бассейне и имеющий по данным УЗДГ двусторонний стеноз ВСА до 70-80% и признаки окклюзии одной из ПА, не может быть прооперирован в плановом порядке до решения вопроса об операции на брахиоцефалах? Т.е. если хирургам надо, то они могут оперировать, но пусть учитывают изначальные операционные риски?
Потом, поступают частенько с уже установленным диагнозом ДЭП 3ст. Для хирургов это первый повод отказать в операции. Я же опять крайний – подтвержу третью ст., значит они откажут, поставлю хотя бы ДЭП 2ст. – другое дело, привет операция. Это что за практика такая?Такое есть где-то в приказах хирургических, может быть?
Сразу оговорюсь, я прекрасно представляю себе эфимерную феменологию диагноза “ДЭП” и отношение уважаемых коллег на данном ресурсе к нему (оно, в общем-то, у меня аналогичное), но тем не менее доказывать что не дурак должен именно я, молодой сотрудник – во всех “букварях” и во всех сторонних заключениях неврологов эти диагнозы цветут и пахнут у всех пациентов старше 50 лет 🙂
Rodionov
19.12.2008, 10:01
Уважаемый коллега! Думаю, что этот документ для Вас:
[Ссылки могут видеть только зарегистрированные и активированные пользователи]
Rodionov
19.12.2008, 11:49
Recommendations
• Promptly examine all stroke patients, and defer nonessential surgery until the evaluation is complete.
• Treat symptomatic carotid stenosis with CEA or CAS before the patient undergoes general or cardiac surgery.
• Allow at least 1 month to elapse between a moderately large ischemic stroke (greater than one third the distribution of the middle cerebral artery) and surgery.
• Asymptomatic carotid bruits and stenoses do not increase the stroke risk for patients who undergo general surgery.
• Carotid bruits and/or stenoses in asymptomatic and symptomatic patients who undergo CABG surgery are associated with a 5% to 7% risk of stroke.
• Symptomatic vertebrobasilar stenosis is associated with a 6% risk of stroke in patients who undergo general surgery or CABG surgery.
• The perioperative stroke risk in patients with intracranial large artery stenosis in the anterior circulation is unknown but is likely to be similar to the risk in symptomatic patients with vertebrobasilar stenosis (6%); the risk is likely to be extremely low in asymptomatic patients.
• Patients with large artery ischemic stroke should undergo an appropriate preoperative cardiac examination.
• Patients with recent symptomatic intracranial large artery stenosis should have surgery delayed for at least 1 month. Intraoperative hypotension must be avoided. There are insufficient data to make a recommendation for prophylactic endovascular revascularization procedures; however, the stroke risk from these procedures likely exceeds the stroke risk in these patients during general surgery.
• Patients with asymptomatic extracranial large artery stenosis do not require CEA or CAS before general surgery; the risks associated with CEA or CAS are higher than the perioperative stroke risk.
• Patients with asymptomatic intracranial arterial stenosis do not require preoperative intervention because the perioperative risks are lower than those for angioplasty and stenting.
Спасибо. Примерно как раз то, что надо.
А не подскажете: нету ли чего-либо подобного в отечественной нормативной базе? Приказы, разъяснения и т.п.?
А то бьют, как известно, по лицу, а не по паспорту, тем более заграничному 🙂
Update:
Прочитал. Не то что примерно, а именно то что надо :). Еще раз большое спасибо.
Но вопрос об отечественной нормативной базе все еще актуален. Как известно, отечественная администрация и отдельные доктора имеют сильный врожденный иммунитет к зарубежным гайдлайнам и иже с ним иноязычным источникам :).
Заранее благодарен.
Rodionov
19.12.2008, 15:39
Еще пару соображений старого консультанта хирургических стационаров.
Строго говоря, требования хирургов/анестезиологов дать заключение в формулировках “противопоказаний нет / противопоказано” неправомочны.
Вы как консультант даете оценку “своему” статусу, даете рекомендации по возможной коррекции риска хирургического вмешательства и оцениваете сам риск.
А дальше фраза типа: Больной получает оптимальную терапию (…такую-то…) цереброваскулярной болезни. Периоперационный риск повторного инсульта такой-то (если можно найти в таблице).
Всё. Пусть хирурги с анестезиологами думают, 5% риск – это много или мало.
Вы сделали для больного всё что могли.
Я знаю консультантов, которые четки стоят на своих позициях и, как правило, через какое-то время взаимопонимание достигается.
Хороший способ – сделать межклиническую (межотделенческую) конференцию, где Вы приводите стратификацию риска, объясняете свою задачу консультанта и договариваетесь о формулировках.
Rodionov
19.12.2008, 15:40
Отечественные кардиологические гайды – это в последние годы – практически полный перевод/пересказ европейских. Ну пару спонсорских препаратов добавят, не более того.
Про неврологию не знаю.
Строго говоря, требования хирургов/анестезиологов дать заключение в формулировках “противопоказаний нет / противопоказано” неправомочны.
Вы как консультант даете оценку “своему” статусу, даете рекомендации по возможной коррекции риска хирургического вмешательства и оцениваете сам риск.
Все верно. Меня например удивляла запись, оставляемая некоторыми консультантами: “противопоказаний для оперативного вмешательства нет”. Как верно сказал sham в одной из тем, пока пациент жив, противопоказаний к операции нет в принципе. Есть только риски – риск, связанный с проведением операции и анестезии и риски связанные с отказом от операции. В каждом случае, вопрос решается индивидуально. Анестезиологический риск, например, будет сильно зависеть от выбранной анестезиологом тактики. Вы ведь не можете знать кто, и как будет проводить пациенту анестезию ? Так что я бы даже воздержался от того, чтобы указывать какие-то проценты.
Источник
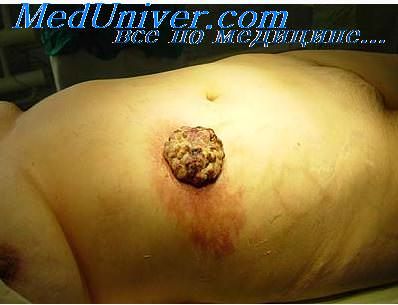
Показания и противопоказания к оперативному лечению опухолей.Показаниями для хирургического лечения являются новообразования небольшого размера — диаметром до 2 см, эпителиальные новообразования кожи, развившиеся на фоне руб-цовой ткани, радиорезистентные опухоли. Как правило, хирургический метод лечения может быть рекомендован при кожном роге, опухолях из придатков кожи, гигантской кондиломе Бушке—Левенштейна, базальноклеточном раке, плоскоклеточном раке кожи и ряде дру гих злокачественных новообразованиях. Частота рецидивирования эпителиальных новообразований кожи после их хирургического иссечения при сроках наблюдения в течение 5 лет варьируется от 6,8 до 41,4%, а при сроке наблюдения до 10 лет — от 16 до 50%. Столь существенные различия в частоте рецидивирования после хирургического метода лечения (хотя это относится и ко всем методам лечения) обусловлены различиями размеров новообразований, клинико-мор-фологических форм, степени инвазии, лока-изации и доступности новообразования для полного хирургического иссечения. Так, при диаметре базалиомы менее 2 см рецидив после хирургического лечения наступает в 0,5%, при диаметре от 2 до 4 см — в 10%, при диаметре, превышающем 4 см, и наличии явлений деструирующего роста в подлежащие тка-ни — в 22% случаев. Чаще всего рецидивирует базальноклеточный рак с краевой инфильтрацией и инфильтрирующие формы со склерозированием опухоли, расположенные на коже носа (40%), щек и периорбиталь-ной области (соответственно 21 и 18%), а также волосистой части головы (10%). Как было отмечено ранее, одним из главных принципов хирургического иссечения эпителиальных новообразований кожи является обязательное иссечение опухоли в пределах здоровой гкани, при базалиоме и кератоакантоме следует отступать на 0,5-1,0 см. а при плоскоклеточном раке кожи и базалиоме типа ulcus rodens — на 1-2 см от края опухоли. В ряде случаев при обширных очагах поражения для закрытия раневого дефекта применяются кожно-пластические операции, которые осуществляются, в основном, путем пересадки кожи на питающем лоскуте или с использованием свободного кожного лоскута. Наиболее часто встречающимся осложнением после хирургического метода лечения является формирование келоидного рубца, который развивается примерно в 11% случаев. С целью предотвращения этого осложнения следует учитывать ряд факторов, способствующих его развитию. В частности, хирургическое вмешательство не следует проводить ранее чем через год после окончания приема изотретиноина. К развитию келоида предрасполагают и анатомические особенности — он чаще развивается после хирургических вмешательств на участках кожи, испытывающих натяжение или непосредственно покрывающих костные выступы, а также на верхней части рук, спины, грудине, плечах, углу нижней челюсти и мочке уха.
Противопоказаниями для хирургического метода лечения эпителиальных новообразований кожи являются сахарный диабет, непереносимость обезболивающих средств, а также невозможность технически полного иссечения опухоли ввиду особой ее локализации (периорбитальная область, нос и ушные раковины). После хирургического удаления опухоли косметический эффект обычно бывает очень хорошим. Однако этот метод не предотвращает развития рецидивов. В частности, после хирургического иссечения рецидивируют от 3.4 до 55% базалиом. Исключительно важным обстоятельством при хирургическом иссечении является использование метода микроскопического контроля краевой зоны опухоли, удаленной в момент оперативного вмешательства. При удалении опухоли под гистологическим контролем удается получить наименьший процент рецидивов — 4,5%. Метод «микрографической хирургии по Мохсу», разработанный в 1936 г. F.E. Mohs, является самым аккуратным методом удаления злокачественной опухоли, обеспечивающим контролируемое серийное микроскопическое исследование ткани, взятой непосредственно у больного и зафиксированной химическим способом in situ при помощи пасты с хлоридом цинка. Ткань для замораживания, получения срезов и последующей микроскопии систематически удаляется по специальной схеме до тех пор пока в срезе не перестают определяться признаки злокачественной опухоли. Методика операции по Мохсу. В зоне расположения опухоли хирургическим лезвием, наклоненным под углом 45°, иссекается блюдцеобразный кусочек ткани. При традиционном хирургическом удалении, в отличие от метода Мохса, разрез проводится перпендикулярно коже. Взятый биоптат разрезается на части, как пирог. Срезы маркируют и помещают в специальный контейнер (чашку Петри) Используя рисованное изображение пациента, составляют карту для точного нанесения участка, откуда была взята ткань опухоли. После этого ткань передают гистологу, который производит гистологические срезы в горизонтальной плоскости таким образом, чтобы ткани, лежащие в глубине, и периферические края кожи вокруг всей опухоли стали доступными для микроскопического исследования. При обнаружении опухоли удаляют дополнительные слои ткани, операция же продолжается до тех пор, пока хирург не достигает слоя, свободного от опухолевых клеток. Процедура «микрографической хирургии по Мохсу» весьма сложна, требует большой точности и специального обучения хирургов. Обычно она проводится амбулаторно, под местной анестезией. Вмешательство может состоять из нескольких циклов. Метод чаще используется при лечении опухолей лица и при других важных в косметическом отношении локализациях, а также при рецидивирующих раках кожи, особенно в случаях, когда раковые клетки продолжают находиться в рубце и границу рецидивирующей опухоли нельзя определить точно. Он показан при склеродермоподобной базалиоме, выбухающей дерматофибросаркоме; базалиоме и плоскоклеточном раке кожи, располагающихся в местах, где велика вероятность рецидива (носогубная складка, внутренний угол глаза, ушная раковина и др.) или в местах, где необходимо максимальное сохранение здоровой ткани (кончики крыло носа, губа, ухо, головка полового члена и др.). – Также рекомендуем “Кюретаж. Электрокоагуляцию.” Оглавление темы “Принципы лечения опухолей кожи.”: |
Источник