Противопоказания при миеломной болезни

Миелома — злокачественная опухоль, подавляющая нормальное кроветворение, разрушающая кости и вырабатывающая патологические белки, повреждающие внутренние органы. Когда говорят о миеломе крови или костей, или позвоночника, или костного мозга, то имеют ввиду одно заболевание с разнообразными проявлениями.
Относящееся к гемобластозам или онкогематологическим процессам, то есть злокачественным болезням крови и лимфатической ткани заболевание имеет много названий: множественная миелома, миеломная болезнь и генерализованная плазмоцитома, плазмоцитарная миелома.
Причина миеломы
Миелома состоит из изменённых плазматических клеток. В нормальном костном мозге плазматические клетки рождаются из В-лимфоцитов, но число их ограничено всего 5%, большее количество — уже патология.
Определённой ясности с первопричиной развития плазматической опухоли нет, в инициации процесса подозревают плохую наследственность и склонность к аллергии против собственных тканей, радиацию и работу с токсичными веществами, под подозрение попал и вирус герпеса 8 типа.
Правда, достоверных доказательств участия всего перечисленного в злокачественном перерождении не представлено. Ясно одно, что-то помешало нормальному созреванию В-лимфоцитов или вмешалось в многоэтапный путь от их «детства» до лимфатической зрелости, из-за чего-то лимфоцит превратился в дефектный плазмоцит, давший начало миеломе.

Миеломная болезнь поражает трёх из 100 тысяч россиян, как правило, пожилых — преимущественно на седьмом десятке жизни, у молодых до 40 лет заболевание встречается очень редко.
Среди страдающих заболеваниями крови и лимфатической ткани плазмоцитому имеет 10-13%, но из всех существующих в природе злокачественных процессов на больных плазмоклеточной опухолью приходится не более одного процента.
Что происходит при миеломе?
По какой-то причине в костном мозге появляются ненормальные клетки, размножаясь, они нарушают нормальное кроветворение, что проявляется анемией. Недостаток эритроцитов сказывается на работе всех органов, но особенно сильно на легочной ткани и головном мозге, что проявляется недостаточностью их функций.
Функция нормальных плазматических клеток — выработка антител-иммуноглобулинов для защиты от болезнетворных агентов. Миеломные плазмоциты тоже вырабатывают иммуноглобулины, но дефектные парапротеины, не способные к иммунной защите.
Вырабатываемые злокачественными плазмоцитами парапротеины откладываются в тканях органов, излюбленное «место складирования» — почки, в которых развивается «болезнь лёгких цепей» с исходом в почечную недостаточность. В поражённой печени снижается выработка разжижающих кровь веществ — повышается вязкость крови, нарушающая обменные процессы в тканях, образуются тромбы. Отложения иммуноглобулинов наносят урон и другим органам, но не столь фатальный.
В костях миеломные клетки стимулируют остеокласты, вызывая остеолизис — разъедание кости. Из разрушенной кости кальций выходит в плазму, накапливаясь, приводит к гиперкальциемии — тяжёлому состоянию, требующему принятия срочных мер.
Диагностика миеломной болезни
Диагноз устанавливается по анализам крови, где находят парапротеины и определяют их суммарную и видовую концентрацию. Парапротеины обозначают как иммуноглобулины — IgA, IgG и IgМ. Плазмоциты вырабатывают иммуноглобулины по собственному усмотрению и в разном количестве, по их изменению продукции патологических белков впоследствии оценивают эффективность лечения и активность заболевания.
Степень агрессивности плазматических клеток выясняют при микроскопии костного мозга, его получают из грудины при стернальной пункции или при биопсии тазовой кости. Особенно актуально исследование при невысокой продукции парапротеинов или при изменении характера течения болезни.
Давний маркёр заболевания — белок Бенс-Джонса в моче, выявляемый у 70% пациентов. Белок формируется из цепочек иммуноглобулинов А и G небольшого молекулярного веса — «лёгких», которые просачиваются из почечных канальцев. По содержания Бенс-Джонса тоже контролируют течение болезни.
Часто заболевание случайно обнаруживается во время обычной рентгенографии органов грудной клетки по литическим дефектам ребер. На первом этапе необходимо выявить все деструктивные изменения в костях, чтобы в дальнейшем следить за процессом и результатами терапии, что позволяет высокочувствительная низкодозная КТ всего скелета.
При МРТ изучается состояние плоских костей — черепа и таза, что обязательно при тлеющей и солитарном варианте опухоли. МРТ помогает оценить не только дефекты кости, но и наличие опухолевой инфильтрации мягких тканей, вовлечение в процесс спинного мозга.
Обязательно проводится анализ на кариотип для выявления генетических аномалий, влияющих на прогноз в отношении жизни больного и эффективность лечения.
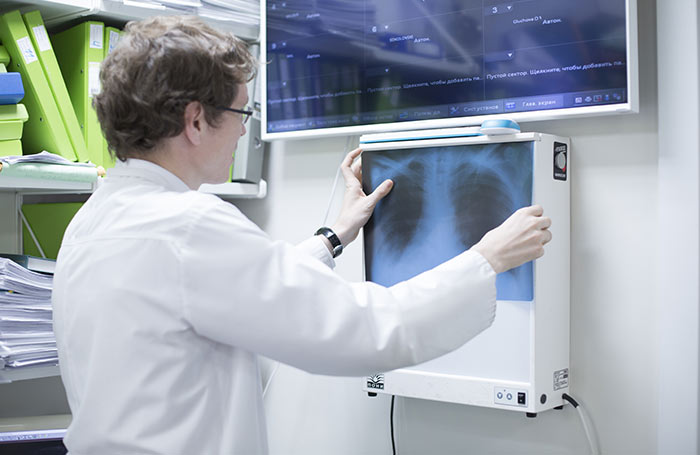
Когда диагноз миеломы не вызывает сомнений
Характерные особенности клеток определяют течение процесса от медленной и практически доброкачественной гаммапатии или тлеющей миеломы до стремительного плазмоклеточного лейкоза.
Не всегда изначально удаётся классифицировать заболевание, что усложняет выбор оптимальной терапии. В 2014 году международный консенсус определил критерии, облегчающие постановку точного диагноза и отделяющие один вариант опухолевого процесса от других.
В первую очередь, в костном мозге определяют процент плазматических клеток, так при симптоматической миеломной болезни их должно быть более 10%, а 60% говорит о высокой агрессивности опухоли.
Для каждого варианта заболевания предусмотрены определенные количественные характеристики и сочетания критериев, так для полной убеждённости в наличии у пациента миеломы необходимо обнаружить специфические «продукты»:
- М-протеин в крови, то есть IgA или IgG;
- легкие цепи иммуноглобулинов;
- в моче белок Бенс-Джонса;
- очаги в костях скелета.
При недостаточности специфических критериев диагностике помогают неспецифические, но часто встречающиеся последствия деятельности плазмоцитов и парапротеинов на органы-мишени:
- повышение уровня кальция крови в результате массивного разрушения костей;
- снижение гемоглобина при опухолевом замещении костного мозга;
- повышение креатинина крови — маркёра почечной недостаточности.
Симптомы миеломы
Замечено, что каждый пул плазматических клеток производит иммуноглобулины с персональными особенностями и по своему графику, отчего клинические проявления очень своеобразны и глубоко индивидуальны. Нет двух одинаковых больных, тем более невозможно найти двух похожих пациентов по диагностическим критериям. Тем не менее, выделяют несколько типов заболевания.
По количеству поражений опухоль может быть генерализованной или множественной и солитарной — с единственным очагом.
По течению различают вялотекущую или тлеющую, она же индолетная, и симптоматическую плазмоцитому, протекающую с явными клиническими проявлениями.

Основное проявление симптоматической миеломы — боли в костях вследствие их разрушения, которые появляются не сразу и часто даже не в первый год заболевания. Болевой синдром возникает при вовлечении в опухолевый процесс надкостницы, пронизанной нервными окончаниями. При медленно текущем процессе до выявления опухоли может пройти несколько лет, поскольку ничего кроме эпизодов слабости у пациента не возникает.
В развёрнутой стадии с множественными поражениями на первый план выходят в разных комбинациях и с индивидуальной интенсивностью переломы в местах деструкции костей и проявления почечной недостаточности, или амилоидоз органов.
Лечение миеломной болезни у молодых
Вялотекущий вариант миеломной болезни не всегда требует лечения, поскольку не угрожает жизни, а терапия совсем не безвредна. В данном случае наблюдение за течением процесса более выгодно пациенту, нежели токсичная химиотерапия. Регулярные обследования позволяют вовремя диагностировать активизацию процесса.
Симптоматическая миелома разделяется по стадиям от I до III по уровню в крови специфического микроглобулина и альбумина, стратегия при стадии I и II-III различается только используемыми препаратами и их комбинациями.
При любой стадии основное и определяющее тактику — состояние пациента и его возраст. Так сохранным больным до 65-летнего возраста и без тяжёлых хронических болезней предлагается агрессивная химиотерапия высокими дозами с пересадкой собственных стволовых клеток крови, по-научному, аутологичной трансплантацией.
Физически сохранные пациенты от 65 до 70-летия тоже могут претендовать на высокодозную химиотерапию, но уже не комбинацией лекарств, а единственным препаратом — мелфаланом.
До начала высокодозной химиотерапии проводится несколько курсов полихимиотерапии обычными дозами, затем специальным препаратом стимулируется выработка костным мозгом собственных стволовых клеток, которые собираются и консервируются. Затем пациент получает очень высокие дозы цитостатиков, в результате чего гибнут все клетки крови — опухолевые и нормальные. Нормальные, заблаговременно законсервированные кровяные элементы и вводят пациенту.
Лечение миеломы у пожилых
Пациенты старше 65 лет и помоложе, но с сопутствующими болезнями, влияющими на общее состояние и активность, тоже на первом этапе проходят цикловую химиотерапию, в том числе с использованием таргетных препаратов. Результат лечения оценивается по анализам крови и костного мозга, где определяют концентрацию специфических для заболевания белков и процент опухолевых клеток.
На результате лечения отражается не только возраст, но и наличие нескольких хронических болезней, астенизация, подразумевающая физическое ослабление с похуданием или без оного.
Астенизированного человека наши предки называли «квёлым». Такие пациенты рискуют не перенести агрессивного лечения, но достаточно неплохо отвечают на более легкие варианты противоопухолевой химиотерапии.
В последние годы спектр химиопрепаратов существенно расширился за счёт таргетных средств, продемонстрировавших хороший непосредственный результат и увеличение продолжительности жизни участников исследований.
Поражения скелета подлежат длительной терапии бисфосфонатами, уменьшающими болевой синдром, предотвращающими переломы и гиперкальциемию. На отдельные опухолевые очаги воздействуют ионизирующим излучением, обязательна лучевая терапия при угрозе сдавления спинного мозга и поражении шейного отдела позвоночника.
Прогноз при миеломной болезни
Кроме возраста пациента и его физического состояния на прогнозе миеломы и продолжительности жизни отражается чувствительность опухоли к лекарственному лечению и биологические характеристики плазматических клеток, в частности генетические аномалии с делецией участков хромосом и амплификацией — удвоением генов.
Играет роль концентрация парапротеинов и их фракций, объем поражения на момент выявления болезни и степень вовлечения в патологический процесс других органов, так уже развившаяся почечная недостаточность «перевесит» все прочие благоприятные признаки заболевания.
Очень важно для жизни пациента правильно выбрать лечащего доктора и клинику, где могут провести точнейшее обследование и пациентом занимается целая команда врачей разных специальностей, знающих клинические проблемы немолодого миеломного больного и умеющих их решать.
Список литературы:
- Давыдов М.И., Аксель Е.М./ Статистика злокачественных новообразований России и странах СНГ 2007 г.//Вестник РОНЦ им. Н.Н. Блохина РАМН, 2009; 20 (3)
- Kyle RA, Rajkumar SV./ Criteria for diagnosis, staging, risk stratification and response assessment of multiple myeloma// Leukemia. 2009; 23(1)
- Durie BGM, Salmon SE. / A clinical staging system for multiple myeloma: Correlation of measure Myeloma cell mass with presenting clinical features, response to treatment, and survival// Cancer, 1975;36.
- Facon T, Mary JY, Hulin C et al./ Melphalan and prednisone plus thalidomide versus melphalan and prednisone or reduced intensity autologous stem cell transplantation in elderly patients with multiple myeloma (IFM 99-06): a randomised trial// Lancet 2007; 370
- Weber DM, Chen C, Nievisky R et al./ Lenalidomide plus dexamethasone for relapsed multiple myeloma in North America.// N Engl J Med 2007; 357.
Источник
Миелома — зло злокачественная опухоль, которая происходит из клеток лимфоидной ткани, а если быть точным — из плазматических клеток. Для нее характерны следующие признаки:
- Инфильтрация костного мозга злокачественным клоном плазматических клеток. В норме в костном мозге располагается около 5 % плазмоцитов, но при миеломе их количество превышает 10%.
- В костях возникают очаги деструкции — из-за токсического действия опухолевых клеток происходит расплавление костной ткани. Это могут быть единичные очаги, либо диффузное поражение.
- В крови и моче обнаруживается специфический белок. У него много названий — М-белок, М-градиент, М-протеин, М-компонент и др. Это моноклональный иммуноглобулин, который имеет высокую молекулярную массу и негативно влияет на весь организм.
Причины миеломной болезни
Причиной миеломы является злокачественное перерождение клеток-предшественниц В-лимфоцитов, при этом образуются специфические мутации. Причины образования данных мутаций пока неизвестны. Пока речь идет только о факторах риска, при наличии которых вероятность развития заболевания увеличивается:
- Мужской пол.
- Возраст старше 40 лет.
- Негроидная раса.
- Наличие в анамнезе моноклональной гаммапатии. У 1% таких пациентов обязательно развивается миелома.
- Наличие вторичных иммунодефицитных состояний. К вторичным иммунодефицитам приводит иммуносупрессивная терапия, показанная при трансплантации органов, химиотерапия при злокачественных заболеваниях, ВИЧ и др.
- Наличие миеломы у кровных родственников.
- Наличие в анамнезе радиационного воздействия, в том числе прохождение лучевой терапии.
Виды миеломы
Миелома представляет разнородную группу заболеваний, часть из которых могут долгое время протекать относительно доброкачественно, а другие приводят к быстрому ухудшению состояния больного.
- Симптоматическая миелома. В данном случае имеется развернутая клиническая картина заболевания, с наличием характерных симптомов и признаков, полученных с помощью инструментального обследования.
- Вялотекущая, или тлеющая миелома. При ней нет повреждения костей, но в плазме крови обнаруживается М-протеин в концентрациях, превышающих 30г/л, или в костном мозге количество плазматических клеток превышает 10%.
- Плазмоцитома. Имеется единичный очаг миеломы в костях (солитарная плазмоцитома), либо во внутренних органах — экстрамедуллярная плазмоцитома.
Есть также редкие варианты множественной миеломы:
- Несекретирующая миелома.
- Биклональная миелома.
- Плазмоклеточный лейкоз и др.
Стадии болезни
1 стадия. Имеется анемия легкой степени (гемоглобин не менее 100г/л), кальций остается в норме, количество очагов остеодеструкции не превышает 5, уровень М-протеина низкий.

2 стадия. Анемия усугубляется, гемоглобин может опуститься до 85г/л, повышается уровень кальция до 3 ммоль/л, увеличивается количество очагов расплавления кости (их уже более 5, но менее 20), повышается уровень М-белка, а в моче определяется протеин Бенс-Джонса в количестве 4-12 г/сутки.
3 стадия выставляется, когда есть хотя бы один из следующих признаков:
- Тяжелая анемия, при которой гемоглобин не превышает 85 г/л.
- Уровень кальция в сыворотке крови превышает 3 ммоль/л.
- Уровень М-протеина более 70 г/л.
- Более 30 остеолитических очагов.
Проявления и осложнения миеломы
Проявление заболевания зависит от его стадии. В некоторых случаях оно может никак не проявлять себя, но по мере нарастания опухолевой массы, заболевание будет прогрессировать. При миеломе возникают следующие симптомы:
- Боли в костях. Сначала они носят периодический характер, могут возникать при изменении положения тела. По мере прогрессирования остеодеструкции, боль становится постоянной и очень сильной. В ряде случаев ее характеризуют как нестерпимую.
- Патологические переломы. Возникают без действия выраженного травмирующего фактора. Поскольку при миеломе происходит остеолизис и резорбция кости, нередки спонтанные переломы. Наиболее опасны переломы позвоночника, поскольку они могут приводить к параличам и парезам.
- При потере костной массы происходит «проседание» позвонков, которое сопровождается ущемлением корешков спинномозговых нервов и развитием неврологической симптоматики — боли, парезы, чувство онемения и даже параличи.
- Увеличение кальция в крови (за счет его выхода из костной ткани). При этом наблюдается тошнота, рвота и общая слабость. При выраженной гиперкальциемии может возникнуть спутанность сознания, сопор и даже кома.
- Поражение почек. М-белок имеет большую молекулярную массу, поэтому «забивает» почечные канальцы, что приводит к развитию почечной недостаточности. Ситуацию усугубляет гиперкальциемия, амилоидоз и инфекционные осложнения, которые характерны для миеломы.
- Когда М-белок в крови превышает 50г/л, развивается синдром гипервязкости крови. Он характеризуется кровотечениями, нарушением зрения и сознания.
- Симптомы, характерные для угнетения мозгового кроветворения: анемии, инфекции, кровотечения.
Рецидивируют ли миеломы
К сожалению, на сегодняшний день миелома является неизлечимым заболеванием. Даже после самого мощного лечения — тандемной высокодозной полихимиотерапии с трансплантацией стволовых клеток все равно развивается рецидив. Задача лечения отсрочить его развитие и затормозить прогрессирование заболевания.
Диагностика миеломы
- Лабораторные анализы:
- Общий анализ крови — определение уровня гемоглобина, подсчет лейкоцитарной формулы. Характерным, но не ключевым признаком миеломы является значительное увеличение СОЭ, у 70% больных оно превышает 30 мм/час, у отдельных пациентов — 100мм/час.
- Анализ мочи — определение уровня общего белка и М-протеина в частности.
- Биопсия костного мозга. Проводится подсчет миелограммы с определением процентного количества плазматических клеток, а также молекулярно-генетические тесты, которые позволяют выявить характерные для миеломы мутации.
- Иммунофенотипирование — позволяет выявить клон опухолевых клеток в пунктате костного мозга.
- Рентгенологические методы исследования, в частности рентген костей или компьютерная томография костей. Эти исследования позволяют выявить очаги остеодеструкции и определить их количество.
- МРТ проводится при наличии неврологической симптоматики для оценки поражения корешков спинномозговых нервов опухолевой массой или разрушенным позвонком. Также МРТ является обязательным исследованием при подозрении на солитарную миелому костей.
Лечение
На сегодняшний день лекарств, которые могли бы полностью излечить миелому, нет. Основные усилия направлены на достижение ремиссии и ее пролонгирование. Схема лечения миеломы будет определяться возрастом пациента и его состоянием. Используется несколько подходов к терапии:
- Стандартная химиотерапия с использованием мелфалана, преднизолона и бортезомиба. Такое лечение миеломы показано ослабленным пациентам и людям старше 65 лет, которые не смогут перенести более серьезное лечение. Для пациентов с тяжелой почечной недостаточностью проводят лечение с использованием бортезомиба и дексаметазона. В ряде случаев дексаметазон можно заменить на преднизолон, чтобы снизить токсическое действие. Также используются схемы лечения, включающие талидомид.
- Высокодозная полихимиотерапия. Наилучшие результаты достигаются при применении высокодозной полихимиотерапии (ВПХ) с последующей трансплантацией гемопоэтических стволовых клеток (ТГСК). Такое лечение показано пациентам младше 65 лет, а также пациентам 65- 70 лет при удовлетворительном состоянии и отсутствии противопоказаний. Возрастные ограничения обусловлены высокими рисками трансплантат-ассоциированной летальности, которая в данном случае может достигать 8%. Почечная недостаточность, даже в терминальной стадии, не является противопоказанием к ВПХ с аутотрансплантацией стволовых клеток при наличии в центре возможностей для проведения гемодиализа.
Схема лечения ВПХТ включает несколько этапов:
1 этап индукционный. На этапе индукции ремиссии рекомендуется применять трехкомпонентные схемы, не включающие мелфарман. Обычно это схемы PAD и VCD, но может использоваться и VD. При достижении полной ремиссии или очень хорошей ремиссии, пациенты направляются в трансплантационный центр для проведения ТГСК. Если опухоль оказалась резистентной, назначают терапию второй линии. Если и после нее нет хорошего эффекта, рассматривают вариант высокодозной полихимиотерапии.

2 этап лечения — трансплантационный. Он, в свою очередь, состоит из нескольких этапов:
- Мобилизация гемопоэтических стволовых клеток (ГСК). На этом этапе необходимо собрать, выделить и заготовить достаточное количество CD 34+. Обычно их выделяют из крови (периферические ГСК), но при необходимости допускается забор из костного мозга. Для мобилизации СК применяется химиотерапия циклофосфаном + гранулоцитарный колониестимулирующий фактор (он провоцирует пролиферацию стволовых клеток). Если не удалось собрать достаточное количество СК, или при проведении повторной мобилизации, вместо циклофосфана используют плериксафор.
- Предтрансплантационное кондиционирование. Этот этап должен начинаться не позже 6 недель после забора ГСК. Его целью является улучшение качества противоопухолевого ответа, которого добились на индукционном этапе. Кондиционирование проводится с использованием высоких доз мелфалана.
- После этого проводится ТГСК, которая для пациента выглядит, как обычное переливание крови.
- При миеломе лечение может включать две ТГСК. Такой режим называется тандемная ТГСК. При этом, повторная трансплантация планируется в период 3-6 месяцев после первой (оптимальные сроки — 3 месяца). Особенно она актуальна для пациентов, не достигших полной ремиссии. Помимо трансплантации собственных СК, по показаниям могут применяться СК донора.
Поддерживающая терапия
Поддерживающая терапия назначается как после ТГСК, так и после стандартной ХТ. Ее целью является уничтожение остаточного клона миеломных клеток. Используется леналидомид или бортезомиб.
Хирургическое лечение при миеломе
Хирургическое лечение используется в качестве паллиативных вмешательств при патологических переломах, компрессии спинного мозга или корешков спинногмозговых нервов . С этой целью проводятся различные реконструктивные операции, призванные устранить компрессию и зафиксировать костные отломки в нужном положении. Также могут быть проведены профилактические операции, при которых кости укрепляют с помощью металлических конструкций, не дожидаясь их переломов.
В ряде случаев при солитарной плазмоцитоме операция может применяться как самостоятельное лечение.
Как узнать, что лечение работает
Для оценки эффективности лечения, разработаны специальные критерии, включающие определение плазматических клеток в костном мозге, М-белка в крови и моче, а также количество очагов остеодеструкции. По этим критериям выделяют следующие формы ответа:
- Полная ремиссия — количество ПК входит в норму и не превышает 5%, в сыворотке и моче отсутствует М-белок, нет новых очагов остеодеструкции.
- Почти полная ремиссия — критерии такие же, как у ПП, но при использовании иммунофиксации в моче определяется М-белок.
- Очень хорошая частичная ремиссия — М-белок в крови снижается на 90% от исходного уровня или определяется только с помощью иммунофиксации.
- Частичная ремиссия — М-белок в крови снижается на 50% от исходного уровня, в моче — на 90%. Если это солитарная плазмоцитома, очаги также должны уменьшится на 50%.
Также могут быть варианты минимального ответа, стабилизации процесса, прогрессирования и развития рецидива.
Что будет, если лечение не дает результатов
Если опухоль резистентна к терапии первой линии, используют препараты второй линии с другим механизмом действия. Например, если в первой схеме применялся бортезумаб, его меняют на леналидомид.
При развитии рецидивов, возможно назначение ХТ первой линии, а также использование препаратов с более высокой противоопухолевой активностью в отношении миеломы — помалидомид, карфилзомиб и др.
Побочные эффекты от лечения миеломы
Побочные эффекты при лечении миеломы аналогичны таковым при любой химиотерапии. Сюда входят:
- Тошнота.
- Рвота.
- Общая слабость.
- Общетоксическое действие.
- Диареи.
- Анемии.
- Иммунодефициты.
- Кровотечения.
Боль при миеломе
Костные боли при миеломе являются очень серьезной проблемой. Для их купирования и предупреждения дальнейшей резорбции кости применяют бисфосфонаты. Препаратом выбора является золедроновая кислота. Также для устранения боли используется лучевая терапия и сильные анальгетики, вплоть до наркотических препаратов.
Продолжительность жизни при болезни
Продолжительность жизни определяется формой заболевания, его стадией и ответом на лечение. Тлеющая миелома может годами не прогрессировать и не угрожать жизни пациента. При активной миеломе средняя продолжительность жизни при 1 стадии составляет 6-7 лет, при 2 стадии — 3-4 года, при 3 — 2 года.
Источник
